
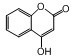
 ��һ��ҽѧ�м��壬�������Ʊ�����Ѫҩ����ͨ������·�ߺϳɣ�
��һ��ҽѧ�м��壬�������Ʊ�����Ѫҩ����ͨ������·�ߺϳɣ�
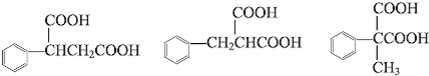 �е�����һ�֣�
�е�����һ�֣�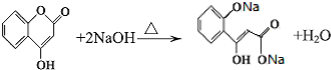
���� A��������Һ��Ӧ���������ɣ���A�д���ȩ���������̿�֪��A��������Ӧ�����������ᣬ��AΪCH3CHO����B��C�Ľṹ��ʽ���Կ�������������е��ǻ�����ԭ��ȡ����������ȡ����Ӧ��D��״���Ũ���������·���������Ӧ����E��E�ĽṹΪ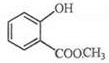 ����F�Ľṹ��ʽ��֪��C��E �ڴ�����������ȥһ��HCl���ӵõ�F��F�д����������ڼ�Һ�п��Է���ˮ�ⷴӦ����϶�Ӧ���ʵ������Լ���ĿҪ������⣮
����F�Ľṹ��ʽ��֪��C��E �ڴ�����������ȥһ��HCl���ӵõ�F��F�д����������ڼ�Һ�п��Է���ˮ�ⷴӦ����϶�Ӧ���ʵ������Լ���ĿҪ������⣮
��� �⣺A��������Һ��Ӧ���������ɣ���A�д���ȩ���������̿�֪��A��������Ӧ�����������ᣬ��AΪCH3CHO����B��C�Ľṹ��ʽ���Կ�������������е��ǻ�����ԭ��ȡ����������ȡ����Ӧ��D��״���Ũ���������·���������Ӧ����E��E�ĽṹΪ ����F�Ľṹ��ʽ��֪��C��E �ڴ�����������ȥһ��HCl���ӵõ�F��F�д����������ڼ�Һ�п��Է���ˮ�ⷴӦ��
����F�Ľṹ��ʽ��֪��C��E �ڴ�����������ȥһ��HCl���ӵõ�F��F�д����������ڼ�Һ�п��Է���ˮ�ⷴӦ��
��1����������ķ�����֪��AΪCH3CHO���ʴ�Ϊ��CH3CHO��
��2������B�Ľṹ��ʽ��B�ĺ��������ŵ��������Ȼ�����C��E��F�Ľṹ��ʽ��֪��C��E����ȡ����Ӧ����F���ʴ�Ϊ���Ȼ���ȡ����Ӧ��
��3������F�Ľṹ��ʽ��֪��F�ķ���ʽ��C10H10O4���÷��ӵ���Է�������Ϊ194������������ʺɱ�Ϊ194���ʴ�Ϊ��C10H10O4��194��
��4����������a����F��Ϊͬ���칹��b��������c�����ڶ�Ԫ����d��������ֻ��һ��ȡ���������F�Ľṹ��ʽ��֪�����������������л����ͬ���칹��Ϊ ����3�֣�
����3�֣�
�ʴ�Ϊ��3�� �е�����һ�֣�
�е�����һ�֣�
��5��G����NaOH��Һ����ʱ��Ӧ�Ļ�ѧ����ʽΪ ��
��
�ʴ�Ϊ�� ��
��
��6����D�����Ȼ��ͷ��ǻ����Ȼ�����NaHCO3��Һ��Ӧ�������ǻ�������NaHCO3��Һ��Ӧ������1molD����1molNaHCO3��Һ��Ӧ���ʢٴ���
��EΪ ���з��ǻ�������E����FeCl3��Һ������ɫ��Ӧ���ʢ���ȷ��
���з��ǻ�������E����FeCl3��Һ������ɫ��Ӧ���ʢ���ȷ��
��BΪ���ᣬ��3�ֵ�Ч�⣬�������ֻ��2���⣬�����ܸ��ݺ˴Ź����������������ǣ��ʢ۴���
�ܸ���G�Ľṹ��ʽ��֪��G��������һ��������һ��̼̼˫��������1molG�������4molH2�����ӳɷ�Ӧ���ʢܴ���
��ѡ�ڣ�
���� ���⿼���л�����ƶϣ�Ϊ�߿��������ͣ��ۺϿ���ѧ����������������ͻ�ѧ֪ʶ���ۺ�������������Ŀ�Ѷ��еȣ�����ע��ע����ϸ���⣬���������Ϣ��


 ���ٴ�����ɽ����ϵ�д�
���ٴ�����ɽ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.4mol | B�� | 0.2mol | C�� | 0.2mol��x��0.4mol | D�� | ��0.2mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | þ�����ᷴӦ��2Fe+6H+�T2Fe3++3H2�� | |
| B�� | �Ȼ�����Һ�м���ͭƬ��Fe3++Cu�TFe2++Cu2+ | |
| C�� | ����ͨ��ˮ�У�CI2+H2O�T2H++CI-+CIO- | |
| D�� | ������Һ�м�������������Һ��2H++SO42-+Ba2++2OH-�TBaSO4��+2H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | ʵ��Ŀ�� | ʵ�鷽�� |
| A | ��֤Br2��������ǿ��l2 | ��������ˮ����Kl��Һ�У��ټ���CCl4�������ã��ɹ۲쵽�²�Һ�����ɫ |
| B | ̽��ʯ���ͷֽ�IJ��ﺬ��ϩ�� | ��ʯ���ͼ�ǿ�Ȳ���������ͨ�����������̼��Һ�� |
| C | ̽������ˮ��IJ������Ƿ��������� | ȡ����������Һ��ϡ���ᣬˮ�ܼ��ȼ����Ӻ��ټ������Ƶ�������ͭ����Һ������ |
| D | ��֤Na���û����������е��� | ��һ��������ˮ�Ҵ��м�������Na������������������ |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 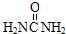 | B�� | H2NCH2CH2NH2 | C�� | ��NH4��2CO3 | D�� | Na2CO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
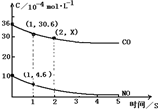 ����������SO2������������NOx�����ǻ�����ѧ�о����ȵ㣮����ͨ��������ԭ��Ӧ����Ӧ���������������
����������SO2������������NOx�����ǻ�����ѧ�о����ȵ㣮����ͨ��������ԭ��Ӧ����Ӧ����������������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
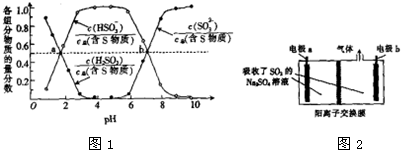
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� |  | B�� |  | C�� | 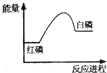 | D�� | 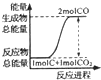 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com