
����Ŀ����֪A��L������������(��Һ�е�����)����F�����������ѧ��ѧ�ﳣ�������ʣ����ǵ�ת����ϵ��ͼ��ʾ(��Ӧ�в��ֲ��Pˮ����ȥ)��
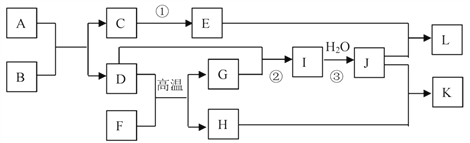
��֪��a.ͨ��״���£�A�ǵ���ɫ���壬B ����ɫ��ζ���壬D �����嵥�ʣ�H �Ǻ���ɫ���壬L�ǰ�ɫ��״������b.��Ӧ���ǹ�ҵ������ͨ�����ķ�Ӧ֮һ����Ӧ�ڢ��ǹ�ҵ����J�IJ��ַ�Ӧ��c. F��������Ԫ����ɵĻ������������Ϊ7��8������д���пհף�
(1)A�ĵ���ʽ__________��
(2)K�Ļ�ѧʽ_____________��
(3)������з�Ӧ����ʽ:
��D+G��I�Ļ�ѧ����ʽ:_____________��
��E+J��L�����ӷ���ʽ��________________��
���𰸡� ![]() Fe2(SO4)3 2SO2+O2
Fe2(SO4)3 2SO2+O2![]() 2SO3 SiO32-+2H+=H2SiO3��
2SO3 SiO32-+2H+=H2SiO3��
��������������������⿼�����ƶϡ�A�ǵ���ɫ���壬B����ɫ��ζ���壬D�����嵥�ʣ�A+B��C+D����Ӧ���ǹ�ҵ������ͨ�����ķ�Ӧ֮һ����AΪNa2O2��BΪCO2��CΪNa2CO3��DΪO2��EΪNa2SiO3��J+Na2SiO3����ɫ��״����L��LΪH2SiO3��J�����ᡣH�Ǻ���ɫ���壬HΪFe2O3����������ת����F![]() G
G![]() I
I![]() J�������볣������������������Ӧ�ڢ��ǹ�ҵ����J�IJ��ַ�Ӧ����֪GΪSO2��IΪSO3��JΪH2SO4��F��������Ԫ����ɵĻ������Ϸ�Ӧ��F+D��O2��
J�������볣������������������Ӧ�ڢ��ǹ�ҵ����J�IJ��ַ�Ӧ����֪GΪSO2��IΪSO3��JΪH2SO4��F��������Ԫ����ɵĻ������Ϸ�Ӧ��F+D��O2��![]() H��Fe2O3��+G��SO2����������Ԫ���غ㣬F�к���Ԫ�غ�SԪ����F��n��Fe����n��S��=
H��Fe2O3��+G��SO2����������Ԫ���غ㣬F�к���Ԫ�غ�SԪ����F��n��Fe����n��S��=![]() ��
�� ![]() =1:2��F�Ļ�ѧʽΪFeS2��
=1:2��F�Ļ�ѧʽΪFeS2��
��1��AΪNa2O2��Na2O2�ĵ���ʽΪ![]() ��
��
��2��HΪFe2O3��JΪH2SO4��H��J��Ӧ�Ļ�ѧ����ʽΪFe2O3+3H2SO4=Fe2��SO4��3+3H2O����K�Ļ�ѧʽΪFe2��SO4��3��
��3��D+G��IΪSO2�Ĵ�������Ӧ����Ӧ�Ļ�ѧ����ʽΪ2SO2+O2![]() 2SO3��
2SO3��
��4��E+J��L�Ļ�ѧ����ʽΪNa2SiO3+H2SO4=Na2SO4+H2SiO3�������ӷ���ʽΪ2H++SiO32-=H2SiO3����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ԫ�������ɺ�Ԫ�����ڱ��������ƶ����������ǣ� ��
A.��35��Ԫ�صĵ����ڳ��³�ѹ����Һ��
B.�������ڵڢ�A���Ԫ��Ϊ�ǽ���Ԫ��
C.�ڶ����ڵڢ�A���Ԫ�ص�����ϼ���+6
D.��������0��Ԫ�ص�ԭ������Ϊ118
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�ϳ���������(��Ҫ�ɷ�ΪAl2O3,SiO2��Fe2O3������)Ϊԭ���Ʊ����⻯�ƣ����⻯��(NaAlH4)���л��ϳɵ���Ҫ��ԭ���������������£�
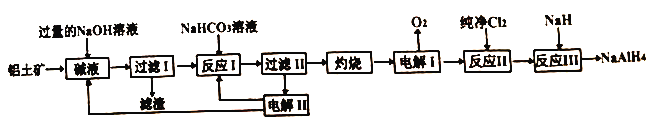 ��֪:SiO2�ڡ���Һ����ת��Ϊ��������Na2Al2SixO8)������
��֪:SiO2�ڡ���Һ����ת��Ϊ��������Na2Al2SixO8)������
(1)����NaOH��Һ�ܽ�������ʱΪ����߽����ʿɲ�ȡ�Ĵ�ʩ��_______��(��дһ��)
(2)���I�Ļ�ѧ����ʽ_______��
(3)�����ա������õ�����Ҫ������_______��_______�����żܡ����������ƾ��ơ�����ǯ��
(4)�����II���ǵ��Na2CO3��Һ��ԭ����ͼ��ʾ��
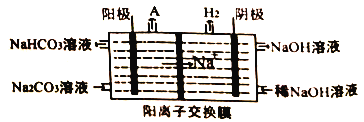
����AΪ_______��(�ѧʽ)
(5)��ӦIII�Ļ�ѧ����ʽΪ_______��ijͬѧ����������Ϊ���������һ�����ۣ����_______ (����������)��Һ������ʵ�ָ������ѭ�����á�
(6)ijͬѧ��Ϊ���Ʊ�����Ҳ���������ܣ��ټ���NaOH��Һ������Һ�������ӳ�����ȫʱ����ʱ��ҺpH��_______��(һ����Ϊ����������Ũ��С��10-5mol/Lʱ������ȫ��Ksp[Fe(OH)3]=1��10-35��Ksp[Al(OH)3]=3��10-34)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������Ǵ�������Ҫ��Ⱦ��ǵ�ǰ������������Ҫ�о�����֮һ��
(1)������ԭ����������
��N2(g)+O2(g)=2NO(g) ��H1 ��4NH3(g)+3O2(g)=2N2(g)+6H2O(l) ��H2
��4NH3(g)+6NO(g)=5N2(g)+6H2O(1) ��H=________��(�ú���H1����H2��ʽ�ӱ�ʾ)
���ݷ�Ӧ�ڣ��ɽ�����ֱ������ȼ�ϵ�أ���KOH��Һ���������Һ��д�������缫��Ӧʽ:____________��
(2)��һ�ܱ�������Ͷ��һ�����İ�����������Ӧ2NH3![]() N2+3H2��H>0����Ӧ������NH3��Ũ����ʱ��仯�������ͼ��ʾ��
N2+3H2��H>0����Ӧ������NH3��Ũ����ʱ��仯�������ͼ��ʾ��
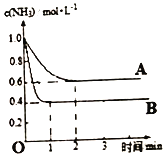
��ش�:
������A�У���Ӧ��ǰ2min��������ƽ����Ӧ����Ϊ________���������µ�ƽ�ⳣ��K=____��
��������������ͬʱ�����ı�ijһ������ʹ�÷�Ӧ������ͼ����B�ķ�Ӧ�����������������Ǹı�_________(�Ũ�ȡ�����ѹǿ�������¶ȡ�������)�������ж�����_________��
(3)һ���¶��£��ں�ѹ�ܱ�������N2O5�ɷ������з�Ӧ:
��2N2O5(g)![]() 4NO2(g)+O2(g) ��2NO2(g)
4NO2(g)+O2(g) ��2NO2(g)![]() 2NO(g)+O2(g)
2NO(g)+O2(g)
����ƽ��ʱ��c(NO2)=0.6mol/L��c(O2)=1.2mol/L����Ӧ����NO2��ת����Ϊ______��N2O5(g)����ʼŨ��Ӧ���ٴ���______mol/L.
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������![]() (x)��
(x)�� (y)��
(y)��![]() (z)�ķ���ʽ��ΪC8H8������˵����ȷ����
(z)�ķ���ʽ��ΪC8H8������˵����ȷ����
A. y�Ķ��ȴ�����3�� B. x��y��z��������ˮ������Ӧ
C. z�е�����ԭ����ͬһƽ���� D. x��ͬ���칹��ֻ��y��z����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�˵����ȷ����
A. һ�������·�ӦN2+3H2![]() 2NH3���ﵽƽ��ʱ��3v��(H2)=2v��(NH3)
2NH3���ﵽƽ��ʱ��3v��(H2)=2v��(NH3)
B. 10mLŨ��Ϊ1mol/L�������������Zn�۷�Ӧ��������������CH3COONa��Һ�����ܽ��ͷ�Ӧ���ʣ��ֲ�Ӱ��H2������
C. ��pH=a+1�İ�ˮϡ��ΪpH=a�Ĺ����У�c(OH��)/c(NH3H2O)��С
D. 25��ʱ��0.1 mol/L��NaHB��Һ�����ԣ�˵��H2BΪǿ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͨ�����ȵ�CuO���ֹ�����ɫ������ռ���һ�ֵ������壬�����������Ӧ�ǣ� ��
A. O2 B. H2 C. NO D. N2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧʵ������һ�ֹ�ҵ�ϵķ���(������Ҫ����MgCO3��MgSiO3������Fe��Al��������)Ϊԭ�ϣ��Ʊ�MgCO3��3H2O��ʵ����������ͼ��ʾ��

��1��Ϊ�˼ӿ�������������ʣ��ɲ�ȡ�İ취��_________(��дһ��)������ʱ��������Ҫ�ɷַ�����Ӧ�����ӷ���ʽΪ___________________________________��
��2������30%H2O2��Ŀ����__________________________________��
��3������ȡ��Һ�ķ�����ȥ��Һ�е�Fe3+
�ټ���30%H2O2������Һ���Ƿ���Fe2+������Լ���__________________________��
����ȡ��Һ��ɺ���ˮ�����Ƿ���Fe3+������Լ���______________________________��
��4�������£���ȥMgSO4��Һ�е�A13+(ʹAl3+Ũ��С��1��10-6mol/L)���������������ʣ�Ӧ������Լ�XΪ__________��Ӧ����pH�ķ�ΧΪ_________________��
��֪����Ksp[Al(OH)3]=1.0��10-33 ��pH=8.5ʱ��Mg(OH)2��ʼ����
��5������Һ�м���Na2CO3��Һ����MgCO3������������ˮϴ�ӣ�ȷ�ϳ���ϴ���IJ�����������____________________________��
��6����ͼΪ��ͬ��Ӧ�¶�������ˮ��̼��þ��X����������ͼ����ͼ��֪������ʱ������¶ȷ�ΧΪ___________________���¶Ƚϸ�ʱMgCO3��3H2O����ת���Ļ�ѧ����ʽΪ_______________________________��

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com