
���� ��1���ɷ���ʽ��֪������C�����ʵ���=�μӷ�ӦA�����ʵ�����ƽ��ʱA�����ʵ���=A����ʼ���ʵ���-�μӷ�Ӧ��A�����ʵ�����
��2�����º�ѹ�£�����ʼʱ����3mol A��3mol B���루1����A��B�����ʵ���֮�Ⱦ�Ϊ1��1����Ϊ��Чƽ�⣬ƽ��ʱ��Ӧ���ת������ͬ��
��3������ʼʱ����x mol A��2mol B��1mol C����ȫת�����������3mol A��3mol B���루1����A��B�����ʵ���֮�Ⱦ�Ϊ1��1����Ϊ��Чƽ�⣬ƽ��ʱ��Ӧ���ת������ͬ�����Եõ�3amol C��
��4���ɣ�3��������֪�����ڣ�3����ƽ���������ټ���3mol C����ЧΪ��ʼ����6mol A��6mol B��
��� �⣺��1���ﵽƽ�������a mol C�����n��A��=��n��C��=amol����A�����ʵ���Ϊ1mol-amol=��1-a��mol��
�ʴ�Ϊ����1-a����
��2�����º�ѹ�£�����ʼʱ����3mol A��3mol B���루1����A��B�����ʵ���֮�Ⱦ�Ϊ1��1����Ϊ��Чƽ�⣬ƽ��ʱ��Ӧ���ת������ͬ����ƽ��ʱ����CΪ��1���е�3����������CΪ3amol��
�ʴ�Ϊ��3a��
��3������ʼʱ����x mol A��2mol B��1mol C����ȫת�����������3mol A��3mol B���루1����A��B�����ʵ���֮�Ⱦ�Ϊ1��1����Ϊ��Чƽ�⣬ƽ��ʱ��Ӧ���ת������ͬ�����Եõ�3amol C��1molCת�����Եõ�1molA��1molB����x=3-1=2��
�ʴ�Ϊ��2��
��4���ɣ�3��������֪�����ڣ�3����ƽ���������ټ���3mol C����ЧΪ��ʼ����6mol A��6mol B���루1������ƽ��Ϊ��Чƽ�⣬ƽ��ʱ��Ӧ���ת������ͬ����ƽ��ʱ����CΪ��1���е�6����������CΪ6amol��
�ʴ�Ϊ��6a��
���� ���⿼�黯ѧƽ���йؼ��㣬�漰��Чƽ�����⣬�ؼ��ǶԵ�Чƽ����ɵ��������գ�


 ��˼ά������ҵ���ټ��ִ�ѧ������ϵ�д�
��˼ά������ҵ���ټ��ִ�ѧ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | �Թ� | B�� | �ձ� | C�� | ��Ͳ | D�� | ��ƿ | ||||
| E�� | ����ƿ | F�� | ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | $\frac{a-b}{a}$ | B�� | $\frac{a}{a+b}$ | C�� | $\frac{2a-b}{a}$ | D�� | $\frac{2a-b}{b}$ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2Na+2H2O�T2NaOH+H2�� | B�� | Fe2O3+3CO$\frac{\underline{\;����\;}}{\;}$2Fe+3CO2 | ||
| C�� | Cl2+2FeCl2�T2FeCl3 | D�� | 3O2$\frac{\underline{\;����\;}}{\;}$2O3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
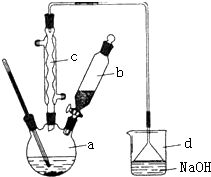 �屽��һ�ֻ���ԭ�ϣ�ʵ���Һϳ��屽��װ��ʾ��ͼ���й��������£������кϳɲ���ش����⣺
�屽��һ�ֻ���ԭ�ϣ�ʵ���Һϳ��屽��װ��ʾ��ͼ���й��������£������кϳɲ���ش����⣺| �� | �� | �屽 | |
| �ܶ�/g•cm-3 | 0.88 | 3.10 | 1.50 |
| �� | 80 | 59 | 156 |
| ˮ���ܽ�� | �� | �� | �� |
 +Br2$\stackrel{����}{��}$
+Br2$\stackrel{����}{��}$ +HBr��
+HBr���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ����һ�о���ѧϰС���ij��ҵ���еĿ�����Ⱦ�����������о���
����һ�о���ѧϰС���ij��ҵ���еĿ�����Ⱦ�����������о����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | A | B | C | D |
| ʵ�� | ��ȥ�Ȼ��ƾ����л��е��Ȼ�茶��� | ����CCl4�е�I2 | ����ƾ���ˮ | ��ȥCO�����е�CO2���� |
| װ�� | 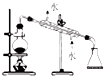 |  |  |  |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com