
| A. | 生成 0.1 NA 根共价键 | B. | 消耗反应物总体积 2.24L | ||
| C. | 转移了 2 NA 个电子 | D. | 产物溶于水后,溶液 pH=1 |
分析 A.1mol HCl中存在1mol共价键;
B.室温下Vm不知,无法计算;
C.据H2+Cl2$\stackrel{点燃}{→}$2HCl~2e-进行计算;
D.据pH=-lgc(H+)进行计算.
解答 解:A.1mol HCl中存在1mol共价键,故0.1mol HCl存在的共价键总数为0.1NA,故A正确;
B.室温下Vm不知,无法计算,故B错误;
C.据H2+Cl2$\stackrel{点燃}{→}$2HCl~2e-
2 2
0.1 0.1,故转移了 0.1 NA 个电子,故C错误;
D.pH=-lgc(H+),由于不知道盐酸的体积,故无法计算氢离子浓度,故D错误.
故选A.
点评 本题考查阿伏加德罗常数,pH的有关计算,题目难度中等,阿伏加德罗常数是高考的“热点”.


科目:高中化学 来源: 题型:实验题

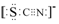 .
.查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 正丁烷与2-甲基丁烷互为同分异构体 | |
| B. | 聚乙烯能使溴的四氯化碳溶液褪色,发生的反应是加成反应 | |
| C. | 苯不能使酸性高锰酸钾溶液褪色,但在FeBr3存在下能与液溴发生取代反应 | |
| D. | 除去乙酸乙酯中残留的乙酸,有效的处理方法是水洗后分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,4.6gNO2和N2O4混合气体中所含原子总数为0.3NA | |
| B. | 4.2g乙烯和丙烯混合气体中含有的极性键数目为0.8NA | |
| C. | 常温下,1L0.5mol/LNH4Cl溶液与2L0.25mol/LNH4Cl溶液所含NH4+的数目相同 | |
| D. | 1mol铁粉在1mol氯气中充分燃烧,转移的电子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Q1>Q2 | |
| B. | 生成物总能量均低于反应物总能量 | |
| C. | 生成 2mol HCl(g)放出 Q1KJ 热量 | |
| D. | 若反应生成 2mol 液态溴化氢,放出的热量低于 Q2KJ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | Y | |
| Z | W |
| A. | X、Y 均能形成不止一种氢化物 | |
| B. | YO 2是一种有毒气体,属于酸性氧化物 | |
| C. | Y 的最简单氢化物比 Z 的稳定性更强 | |
| D. | XW2中各原子最外层均达到 8e-稳定结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
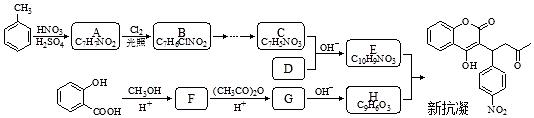
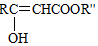
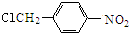 $→_{△}^{NaOH水溶液}$
$→_{△}^{NaOH水溶液}$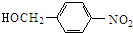 $→_{催化剂}^{O_{2}}$
$→_{催化剂}^{O_{2}}$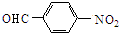 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com