
【题目】某酸HX是一元弱酸,25℃时的电离平衡常数K a= 4.0×10—8。
(1)写出该酸的电离方程式_____________,其电离平衡常数表达式K a =_______。
(2)25℃时,向1 mol·L-1 HX 溶液中加入1 mol·L-1 盐酸,会________(“抑制”或“促进”)HX的电离,c(H+)____________(填“增大”、“减小”或“不变”), 电离平衡常数K a ________(填“增大”、“减小”或“不变”)。
(3)25℃时,若HX的起始浓度为0.01 mol·L-1,则平衡时c(H+)=_________mol/L, 由水电离的出的c(H+)=___________mol/L。
【答案】HA![]() H++A—
H++A— ![]() 抑制 增大 不变 2.0×10—5 5.0×10—10
抑制 增大 不变 2.0×10—5 5.0×10—10
【解析】
某酸HX是一元弱酸,HX在溶液中部分电离,向1 mol·L-1 HX 溶液中加入1 mol·L-1 盐酸,溶液中氢离子浓度增大,电离平衡向左移动,抑制醋酸电离,温度不变,电离常数Ka不变。
(1)某酸HX是一元弱酸,HX在溶液中部分电离,电离方程式为HA![]() H++A—,电离平衡常数表达式Ka=
H++A—,电离平衡常数表达式Ka=![]() ,故答案为:HA
,故答案为:HA![]() H++A—;
H++A—;![]() ;
;
(2)25℃时,向1 mol·L-1 HX 溶液中加入1 mol·L-1 盐酸,溶液中氢离子浓度增大,电离平衡向左移动,抑制醋酸电离,温度不变,电离常数Ka不变,故答案为:抑制;增大;不变;
(3)25℃时,若HX的起始浓度为0.01 mol·L-1,由电离平衡常数表达式Ka=![]() 可知,溶液中c(H+)=
可知,溶液中c(H+)=![]() =
=![]() =2.0×10—5 mol/L,由水电离的出的c(H+)=c(OH—)=
=2.0×10—5 mol/L,由水电离的出的c(H+)=c(OH—)=![]() =
=![]() =5.0×10—10mol/L,故答案为:2.0×10—5;5.0×10—10。
=5.0×10—10mol/L,故答案为:2.0×10—5;5.0×10—10。


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:
【题目】下列有关苯 (![]() ) 与(3)-轴烯 (
) 与(3)-轴烯 (![]() )的说法错误的是
)的说法错误的是
A.二者互为同分异构体
B.二者可用酸性KMnO4溶液鉴别
C.(3)-轴烯与足量H2反应所得产物的二氯代物有5种
D.苯分子中所有原子共平面,(3)-轴烯分子中所有原子不可能共平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨所需的氢气可用煤和水作原料经多步反应制得,其中的一步反应为:CO(g)+H2O(g) ![]() CO2(g)+H2(g) ΔH<0。反应达到平衡后,为提高CO的转化率,下列措施中正确的是( )
CO2(g)+H2(g) ΔH<0。反应达到平衡后,为提高CO的转化率,下列措施中正确的是( )
A.增大CO的浓度B.降低温度C.升高温度D.增大压强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将2.32g碳酸钠、氢氧化钠的固体混合物完全溶解于水,制成溶液,然后向该溶液中逐滴加入1mol/L的盐酸,所加盐酸的体积与产生CO2的体积(标准状况)关系如下图所示,下列说法中正确的是( )
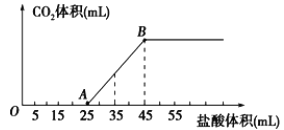
A.OA段发生反应的离子方程式为:H++OH-→H2O
B.B当加入35mL盐酸时,产生CO2的体积为224mL
C.A点溶液中的溶质为NaC1、Na2CO3
D.混合物中NaOH的质量0.60g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨是最重要的氮肥,是产量最大的化工产品之一。其合成原理为:N2(g)+3H2(g) ![]() 2NH3(g) ΔH=-92.4kJ·mol-1。在密闭容器中,使2molN2和6molH2混合发生上述反应:
2NH3(g) ΔH=-92.4kJ·mol-1。在密闭容器中,使2molN2和6molH2混合发生上述反应:
(1)当反应达到平衡时,N2和H2的浓度比是____;N2和H2的转化率比是____。
(2)升高平衡体系的温度(保持体积不变),混合气体的平均相对分子质量___________,密度______。(填“变大”“变小”或“不变”)。
(3)若容器恒容、绝热,加热使容器内温度迅速升至原来的2倍,平衡将_____(填“向左移动”“向右移动”或“不移动”)。达到新平衡后,容器内温度_____(填“大于”“小于”或“等于”)原来的2倍。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.一个CsCl晶胞中含有8个Cl-。
B.离子晶体类的物质均是电解质,故离子晶体均能导电。
C.锗和碳都存在具有原子晶体结构的单质,锗和碳都易形成四个键,能形成原子晶体结构。
D.某物质是由X(黑球)、Y(白球)两种微粒构成的,它们在二维平面中的排列情况为![]() ,则该物质化学式为XY2。
,则该物质化学式为XY2。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】东晋《华阳国志·南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)闻名中外,曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
(1)镍元素基态原子的电子排布式为______,3d能级上的未成对电子数为_______。
(2)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。
①[Ni(NH3)6]SO4中阴离子的立体构型是________。
②在[Ni(NH3)6]SO4中Ni2+与NH3之间形成的化学键称为______,提供孤电子对的成键原子是______。
③氨的沸点_______(填“高于”或“低于”)膦(PH3),原因是_______;氨是______分子(填“极性”或“非极性”),中心原子的轨道杂化类型为_______。
(3)铜晶体铜碳原子的堆积方式如图所示。
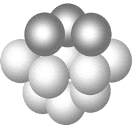
①基态铜在元素周期表中位置__________________。
②每个铜原子周围距离最近的铜原子数目_________。
(4)某M原子的外围电子排布式为3s23p5,铜与M形成化合物的晶胞如图所示(黑点代表铜原子)。
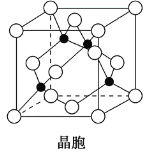
①该晶体的化学式为__________________。
②已知铜和M的电负性分别为1.9和3.0,则铜与M形成的化合物属于________(填“离子”或“共价”)化合物。
③已知该晶体的密度为ρ g·cm-3,阿伏加德罗常数为NA,则该晶体中铜原子和M原子之间的最短距离为________pm(只写计算式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以![]() 表示阿伏加德罗常数,下列说法中正确的是
表示阿伏加德罗常数,下列说法中正确的是
A.58.5 g氯化钠固体中含有![]() 个氯化钠分子
个氯化钠分子
B.1 mol Fe参与反应失去电子数目一定为2![]()
C.1 molNa被完全氧化生成Na202,失去2![]() 个电子
个电子
D.常温下,46 g N02和N204的混合物中含有的氮原子数为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁和铜都是日常生活中常见的金属,有着广泛的用途。请回答下列问题:
(1)配合物Fe(CO)x常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)x晶体属于__________(填晶体类型);Fe(CO)x的中心原子价电子数与配体提供电子数之和为18,则x=_____________;![]() 的核外电子排布式为_____________________。
的核外电子排布式为_____________________。
(2)![]() 溶液可用于检验_________(填离子符号);
溶液可用于检验_________(填离子符号);![]() 中碳原子杂化轨道类型为_____;1mol
中碳原子杂化轨道类型为_____;1mol![]() 含有的π键数目为_______(用N表示);C、N、O第一电离能由大到小的顺序为_________(用元素符号表示)。
含有的π键数目为_______(用N表示);C、N、O第一电离能由大到小的顺序为_________(用元素符号表示)。
(3)某M原子的外围电子排布式为![]() ,铜与M形成的某化合物的晶胞结构如下图所示(黑点代表铜原子)。
,铜与M形成的某化合物的晶胞结构如下图所示(黑点代表铜原子)。
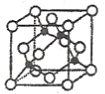
①该晶体的化学式为__________________。
②已知铜和M的电负性分别为1.9和3.0,则铜与M形成的化合物属于___________(填“离子”或“共价”)化合物。
③已知该晶体的密度为![]() ,阿伏加德罗常数为
,阿伏加德罗常数为![]() ,则该晶体中铜原子和M原子之间的最短距离为____________________pm(只需写出计算式)。
,则该晶体中铜原子和M原子之间的最短距离为____________________pm(只需写出计算式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com