
����Ŀ��������ʾ��dz��ɫ��FeSO4��7H2O����ʧˮΪFeSO4��H2Oʱ�ʰ�ɫ����FeSO4ʱΪ��ɫ���塣FeSO4�����ȿɷֽ�ΪFeO��SO3����ǿ�ȿɷֽ�ΪFe2O3��SO3��SO2��SO3���۵�Ϊ16.8�����е�Ϊ44.8������ѧ��ȤС����������Ͻ���ʵ��̽����
��һ�������̷�����ˮ����������
��1����ҩƷװ��������д���ƣ�____�н��м��ȣ��ѽ��ᾧˮ�����������ǣ�ѡ����ţ�___��
A���۲���ˮ�������� B�������ز���������γ������õ���������ȫ��ͬ
C��������ȫ��Ϊ��ɫ D�������ز���������������������ƽ�������
�ڶ�����ȡһ������ˮ��������������ͼ�����ּг�������ȥ����ʾA���Թ��н��м��ȡ�
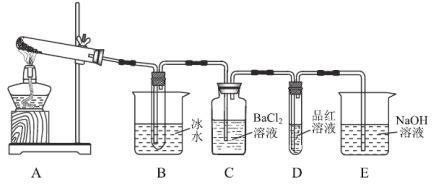
��2��ʵ�������C��D��E�г�������������������������������B�Թ��в�����������������ˮ���������Һ�е������ӵķ����ǣ�___��ʵ������л���һ�����Ե������ǣ�________________��
�����������ڶ���ʵ���װ����A��B���ָ�Ϊ��ͼ��ʾ��![]() ��
��![]() ��C��D��E���䣨C��E�ж�װ��������Һ����
��C��D��E���䣨C��E�ж�װ��������Һ����
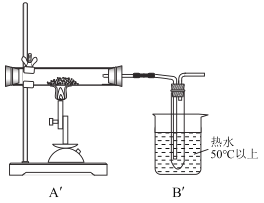
ͬ��ȡһ������ˮ������������![]() ��ʯӢ�������н��м��ȣ���Ӧ��Ϻ�ʯӢ�������������������ž����۲쵽C�в�����ɫ������D�Թ�����Һ��ɫ��
��ʯӢ�������н��м��ȣ���Ӧ��Ϻ�ʯӢ�������������������ž����۲쵽C�в�����ɫ������D�Թ�����Һ��ɫ��
��3��ʵ����![]() �IJ������е������ǣ�______��˵��
�IJ������е������ǣ�______��˵��![]() װ�õ�һ�������ǣ�________��
װ�õ�һ�������ǣ�________��
���C��Һ����ȫȡ�����й��ˡ�ϴ�ӡ�����Ƶ����ù�������Ϊ23.300g��������Һ��ˮϡ�Ͷ���Ϊ1L��ȡ��20.00mL������ƿ�У�����֪Ũ�ȵı�NaOH��Һ�ⶨ��1L��Һ��һ�����ʵ�Ũ�ȡ�
��4������ʵ��������õ��Ķ���������_______���õ���ָʾ����_______��
��5����������Һ��ˮ����ʱ����ˮ���õ���������Ϊ_____����ȥ����![]() �������в������������Ӧ�ӽ���____g��
�������в������������Ӧ�ӽ���____g��
���𰸡����� D ȡ���������Ȼ�����Һ������ɫ������������������� A���Թ�����ɫ�����Ϊ��ɫ��ĩ ��ɫ�����Ϊ��ɫ��ĩ ��ֹC����Һ������![]() �������У����ֹSO3������Һ̬���̬�� 1000mL����ƿ���ζ��ܡ�������ƽ ��̪��Һ ��ͷ�ι� 16.000g
�������У����ֹSO3������Һ̬���̬�� 1000mL����ƿ���ζ��ܡ�������ƽ ��̪��Һ ��ͷ�ι� 16.000g
��������
�������⣬�̷���FeSO4��7H2O������ʧˮΪFeSO4��H2Oʱ�ʰ�ɫ����FeSO4ʱΪ��ɫ���塣FeSO4�����ȿɷֽ�ΪFeO��SO3����ǿ�ȿɷֽ�ΪFe2O3��SO3��SO2������SO42-�ķ����ǣ�ȡ���������Ȼ�����Һ������ɫ������������������ӣ�C�зֽ����ɵ�SO3��BaCl2��Һ��Ӧ�������ᱵ���������ᣬ�Դ˽��з������
��1�����չ�����Ҫ�������н��У�����ʧˮ���������ù���ɷ�ΪFeSO4����������γ��������������ƽ���������ȷ�����ᾧˮ�ѳ�������ѡD������ѡ�������ȷ��
��ˣ�������ȷ���ǣ�������D��
��2��FeSO4�����ȿɷֽ�ΪFeO��SO3����ǿ�ȿɷֽ�ΪFe2O3��SO3��SO2��ʵ�������C��D��E�г���������������������������˵��û����SO2��B�Թ��в�������������ΪSO3������ˮ�õ����ᣬ����SO42-�ķ����ǣ�ȡ���������Ȼ�����Һ������ɫ������������������ӣ�FeSO4�����ȿɷֽ�ΪFeO��SO3��FeOΪ��ɫ��ĩ����A���Թ�����ɫ�����Ϊ��ɫ��ĩ��
��ˣ�������ȷ���ǣ�ȡ���������Ȼ�����Һ������ɫ������������������ӣ�A���Թ�����ɫ�����Ϊ��ɫ��ĩ��
��3��FeSO4��ǿ�ȿɷֽ�ΪFe2O3��SO3��SO2��ʵ����![]() �IJ������е������ǣ���ɫ�����Ϊ��ɫ��ĩ��
�IJ������е������ǣ���ɫ�����Ϊ��ɫ��ĩ��![]() װ�õ��Թ�����ˮԡ���ȣ�������ȫƿ�����ã���ֹC����Һ������
װ�õ��Թ�����ˮԡ���ȣ�������ȫƿ�����ã���ֹC����Һ������![]() �������У�Ҳ���Է�ֹSO3������Һ̬���̬��
�������У�Ҳ���Է�ֹSO3������Һ̬���̬��
��ˣ�������ȷ���ǣ���ɫ�����Ϊ��ɫ��ĩ����ֹC����Һ������![]() �������У����ֹSO3������Һ̬���̬����
�������У����ֹSO3������Һ̬���̬����
��4��C�зֽ����ɵ�SO3��BaCl2��Һ��Ӧ�������ᱵ���������ᣬ���˳�������ϴ�ӡ����������������Һ�������ᣬ��ˮϡ�Ͷ���Ϊ1L��ȡ��20.00mL������ƿ�У�����֪Ũ�ȵı�NaOH��Һ�ⶨ�����ϲ����õ��Ķ���������1000mL����ƿ���ζ��ܡ�������ƽ����NaOH�������ѡ�÷�̪Ϊָʾ����
��ˣ�������ȷ���ǣ�1000mL����ƿ���ζ��ܡ�������ƽ����̪��Һ��
��5������ʱ��ˮ���õ���������Ϊ��ͷ�ιܣ�
�ɷ�Ӧʽ2FeSO4![]() Fe2O3+SO3��+SO2����֪�����ɵ����ʵ�����Fe2O3��SO3��
Fe2O3+SO3��+SO2����֪�����ɵ����ʵ�����Fe2O3��SO3��
����SO3~BaSO4���ɼ����n(Fe2O3)=n(SO3)=n(BaSO4)=![]() =0.1000mol��
=0.1000mol��
![]() �������в�������ΪFe2O3��������ӦΪ0.1000mol��160g/mol=16.000 g��
�������в�������ΪFe2O3��������ӦΪ0.1000mol��160g/mol=16.000 g��
��ˣ�������ȷ���ǣ���ͷ�ιܣ�16.000g��


 ÿ��10���ӿ�����������������ϵ�д�
ÿ��10���ӿ�����������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�������£��������������������Ӧ��2SO2(g)��O2(g) ![]() 2SO3(g)��
2SO3(g)��
��1�������¶ȣ���ѧ��Ӧ����________(����������������С��������������)��
��2��600 ��ʱ����һ�ݻ�Ϊ2 L���ܱ������У������������������ϣ��ڷ�Ӧ������10 min��20 minʱ���ֱ�ı���Ӱ�췴Ӧ��һ����������Ӧ������SO2��O2��SO3���ʵ����仯��ͼ��ʾ��ǰ10 min����Ӧ������____(����������������С������������)��ǰ15 min����SO3��ʾƽ����Ӧ����Ϊ________��

��3��ͼ�з�Ӧ���̣���ʾ����Ӧ�������淴Ӧ������ȣ����ﵽƽ��״̬����ʱ�����_____________��
��4��������ͼ�жϣ�10 minʱ�ı������������_______________________________(ѡ�������ţ���ͬ)��20 minʱ�ı�ķ�Ӧ����������________��
a��������� b����С�����ݻ�
c�������¶� d������O2��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����в����У���������������
A. ��ʱ��ƿ��Һ�彦��
B. �ζ���������ˮϴ��ֱ��ע���Һ
C. ����ʱ��ʼ���ӣ���ֹʱ����
D. ��ƿ��ϴ����������������ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪(CN)2�������Ա�Br2������I2ǿ��NaCN��ˮ��Һ�ʼ��ԣ��������йر仯һ�㲻�ܷ�������
A. CH2=CH2+(CN)2��NC-CH2-CH2-CN
B. (CN)2+2Br-��2CN-+Br2
C. (CN)2+2OH-��CN-+CNO-+H2O
D. HCN![]() H++CN-
H++CN-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʱ��CH3COOH�ĵ���ƽ�ⳣ��ΪK����20mL 0.1mol/L CH3COOH��Һ����μ���0.1mol/L NaOH��Һ����pH�仯������ͼ��ʾ�������¶ȱ仯��������˵������ȷ���ǣ� ��
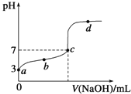
A. b���ʾ����Һ��c(Na+)��c(CH3COO��)
B. c���ʾCH3COOH��NaOHǡ�÷�Ӧ��ȫ
C. d���ʾ����Һ��c(CH3COO��) c(H+)/c(CH3COOH)����K
D. b��c��d�����ʾ����Һ��һ�������ڣ�c(Na+)+c(H+)�Tc(CH3COO��)+c(OH��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����淴Ӧ��2NO2(g)![]() 2NO(g)+O2(g)�ں����ܱ������з�Ӧ���ﵽƽ��״̬�ı�־�Ǣٵ�λʱ��������n molO2 ��ͬʱ���� 2n mol NO���ڵ�λʱ��������2n molNO2��ͬʱ����n molO2���ۻ���������ɫ���ٸı��״̬����2v(NO2)��= v(O2)�����ݻ�������ƽ����Է����������ٸı��״̬�����������ܶȲ��ٸı��״̬
2NO(g)+O2(g)�ں����ܱ������з�Ӧ���ﵽƽ��״̬�ı�־�Ǣٵ�λʱ��������n molO2 ��ͬʱ���� 2n mol NO���ڵ�λʱ��������2n molNO2��ͬʱ����n molO2���ۻ���������ɫ���ٸı��״̬����2v(NO2)��= v(O2)�����ݻ�������ƽ����Է����������ٸı��״̬�����������ܶȲ��ٸı��״̬
A. �٢ۢ� B. �ڢܢ� C. �٢ۢܢ� D. �٢ڢۢܢݢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͼ��ʾԭ���װ�õ���������ȷ����
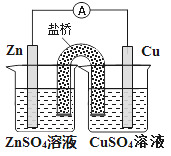
A. ͭ��������ͭƬ�������ݲ���
B. пƬ��������
C. ���Ӵ�ͭƬ����������пƬ
D. ��������������ZnSO4��Һ�ƶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʾ���ʵ��Ʊ�������������
A. ʵ���ҴӺ�������ȡ���ʵ�ȡ�����������ܽ�����������ȡ������
B. ���ʯ(��Ҫ�ɷ�TiO2)Ϊԭ����������Ti�����ʯ����̿![]() TiCl4
TiCl4![]() Ti
Ti
C. ��±ˮ��(������Ҫ��MgCl2)��ȡMg
±ˮ![]() Mg(OH)2
Mg(OH)2![]() MgCl2(aq)
MgCl2(aq) ![]() MgCl(s)
MgCl(s) ![]() Mg
Mg
D. ��ʳ����ȡƯ�۾�NaCl(ag) ![]() Cl2
Cl2![]() Ư�۾�
Ư�۾�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪![]() (X)��
(X)��![]() (Y)��Ϊͬ���칹�壬����˵������ȷ����
(Y)��Ϊͬ���칹�壬����˵������ȷ����
A. Y��һ�ȴ���ֻ������
B. X������ԭ�ӿ��ܴ���ͬһƽ��
C. X��Y������������ȫ�ӳ�ʱ�������������ʵ���֮��Ϊ1��1
D. X��Y����ʹ���ˮ��Һ��ɫ������ɫ��ԭ����ͬ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com