
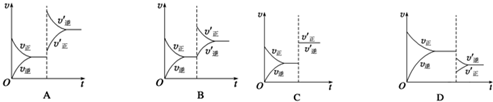
分析 (1)加入催化剂,正逆反应速率同时增大,且增大幅度相同,催化剂不影响化学平衡;
(2)该反应为放热反应,升高温度,正逆反应速率都增大,由于平衡向着逆向移动,逆反应速率增大幅度大于正反应速率;
(3)增大反应容器体积,减小了压强,正逆反应速率都减小,平衡向着体积增大的逆反应方向移动.
解答 解:(1)催化剂只影响反应速率,不影响化学平衡,所以加入催化剂后正逆反应速率同时增大且相等,化学平衡不发生移动,所以C正确;
故答案为:C;不;
(2)升高温度后,正反应速率和逆反应速率都增大,由于该反应为放热反应,平衡向着逆反应方向移动,说明逆反应速率大于正反应速率,所以A正确,
故答案为:A;逆反应;
(3)该反应为体积缩小的反应,增大反应容器体积,反应体系压强减小,正逆反应速率都会减小,平衡向着体积增大的逆反应方向移动,说明逆反应速率减小幅度减小,即逆反应速率大于正反应速率,满足该变化的图象为D,
故答案为:D.
点评 本题考查外界条件对化学平衡的影响,题目难度中等,解决这类题目的关键是分析改变条件的瞬间,正、逆反应速率的变化及变化幅度.


科目:高中化学 来源: 题型:选择题
| A. | H2O与D2O互称同素异形体 | |
| B. | 1H与D互称同位素 | |
| C. | 氘(D)原子核外有1个电子 | |
| D. | 1H218O与D216O的相对分子质量相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同周期X、Y、Z元素的最高价含氧酸的酸性:HXO4>H2YO4>H3ZO4,则气态氢化物还原性HX<H2Y<ZH3 | |
| B. | 元素R的含氧酸的化学式是H2RO3,则其气态氢化物的化学式就是RH4 | |
| C. | 金属与非金属元素分界线附近的元素是过渡元素 | |
| D. | 物质的量相同的Na+、O2-、NH3三种微粒,一定含有相同的质子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 肯定是x+2 | B. | 肯定是x+2或x+8或x+32 | ||
| C. | 肯定是x+2或x+12或x+26 | D. | 肯定是x+2或x+10或x+26 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL) | 50 | 120 | 232 | 290 | 310 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
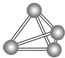 意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意义的N4气体分子.N4分子结构如图所示,下列说法正确的是( )
意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意义的N4气体分子.N4分子结构如图所示,下列说法正确的是( )| A. | N4分子属于一种新型的化合物 | B. | N4分子中只含有共价键 | ||
| C. | 1 mol N4分子所含共价键数为4NA | D. | N4沸点比P4(白磷)高 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol•L-1盐酸的澄清透明溶液:Fe3+、Na+、SO42-、Br- | |
| B. | pH=1的溶液中:Na+、K+、MnO4-、HCO3- | |
| C. | 能使石蕊变红的溶液:Cu2+、Na+、AlO2-、Cl- | |
| D. | c(H+)=1×10-13mol/L的溶液中:Mg2+、Cu2+、SO42-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 如图是Ca(0H)2在水中的溶解度随温度变化的曲线,下列说法不正确的是( )
如图是Ca(0H)2在水中的溶解度随温度变化的曲线,下列说法不正确的是( )| A. | a点和b点的Ksp:a<b | |
| B. | 向溶液a中加入CaO并恢复原温度时,溶液的pH不变 | |
| C. | b点时,Ca(OH)2在水中和在NaOH溶液中的溶解度:s(H2O)>s(NaOH) | |
| D. | 溶解速率:b点>a点 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
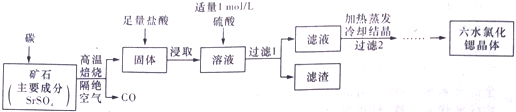
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com