
科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源:2016届安徽省宿州市高一上学期期末考试化学试卷(解析版) 题型:实验题
下图为配制0.2mol·L-1Na2CO3溶液250mL示意图。

回答下列问题:
(1)①中称得Na2CO3_____________g。
(2)玻璃棒在②、③两步中的作用分别是_____________、_____________。
(3)若出现如下情况,对所配溶液浓度有何影响?(填“偏高”、“偏低”或“无影响”)
A.某同学在第⑧步观察液面时俯视_____________;
B.没有进行操作步骤④和⑤_____________;
C.在第⑤步不慎有少量液体流到容量瓶外_____________。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年江西省景德镇市高一上学期期中考试化学试卷(解析版) 题型:实验题
下图是硫酸试剂瓶标签上的内容。
|
硫酸:化学纯(CP)(500mL) 品名:硫酸 化学式:H2SO4 相对分子质量:98 密度:1.84g·cm-3 质量分数:98% |
(1)该硫酸的物质的量浓度为 ;
(2)实验室用该硫酸配制240mL 0.46mol/L的稀硫酸,则
①有以下仪器: A.烧杯 B.100mL量筒 C.250mL容量瓶 D.500mL容量瓶 E.玻璃棒 F.托盘天平(带砝码)G.10mL量筒H.胶头滴管,配制时,必须使用的仪器有 (填代号).
②需要该硫酸的体积为 mL.
③下图为配制过程中的几个关键步骤和操作:将上述实验步骤A—F按实验过程
先后次序排列 。
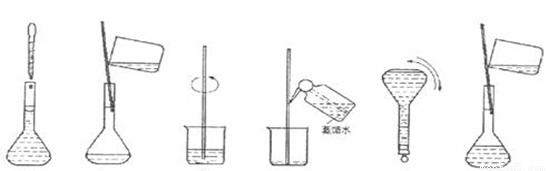
A B C D E F
④该同学实际配制得到的浓度为0.45mol/L,可能的原因是
A.量取浓H2SO4时仰视刻度
B.容量瓶洗净后未经干燥处理
C.没有将洗涤液转入容量瓶
D.定容时仰视刻度
查看答案和解析>>
科目:高中化学 来源:2014届吉林省长春市高一下学期期初考试化学试卷(解析版) 题型:选择题
化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的。如下图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化:

下列说法正确的是( )
A.1 mol N2(g)和1 mol O2(g)反应放出的能量为180 kJ
B.1 mol N2(g)和1 mol O2(g)具有的总能量小于2 mol NO(g)具有的总能量
C.通常情况下,N2(g)和O2(g)混合能直接生成NO
D.NO是一种酸性氧化物,能与NaOH溶液反应生成盐和水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com