
| A. | 金属钠在空气中加热,生成淡黄色固体:2Na+O2$\frac{\underline{\;\;△\;\;}}{\;}$Na2O2 | |
| B. | 向硫酸铝溶液中加入氨水制备氢氧化铝:Al3++3NH3•H2O═Al(OH)3 ↓+3NH4+ | |
| C. | 铁在潮湿的环境中生锈:3Fe+4H2O═Fe3O4+4H2↑ | |
| D. | 二氧化氮溶于水有硝酸生成:3NO2 +H2O═2HNO3+NO |
分析 A.钠在空气中燃烧生成过氧化钠;
B.氨水为弱碱,硫酸铝与氨水反应生成氢氧化铝沉淀和硫酸铵;
C.铁生锈生成氧化铁和氢气,不是生成四氧化三铁;
D.二氧化氮与水反应生成硝酸和一氧化氮气体.
解答 解:A.金属钠在空气中加热,生成淡黄色固体过氧化钠,反应的化学方程式为:2Na+O2$\frac{\underline{\;\;△\;\;}}{\;}$Na2O2,故A正确;
B.向硫酸铝溶液中加入氨水制备氢氧化铝,反应的化学方程式为:Al3++3NH2•H2O═Al(OH)3 ↓+3NH4+,故B正确;
C.铁锈的主要成分为氧化铁,不会生成氢气,正确的化学方程式为:2Fe+3O2═Fe2O3,故C错误;
D.二氧化氮溶于水生成硝酸和一氧化氮,反应的化学方程式为:3NO2 +H2O═2HNO3+NO,故D正确;
故选C.
点评 本题考查了化学方程式的书写及其应用,题目难度中等,明确发生反应实质为解答关键,C为易错点,注意铁锈的主要成分为三氧化二铁,不是四氧化三铁.


 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源: 题型:选择题
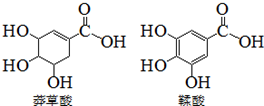 莽草酸是一种合成药物达菲的原料,鞣酸存在于苹果、生石榴等植物中.下列关于这两种有机化合物的说法正确的是( )
莽草酸是一种合成药物达菲的原料,鞣酸存在于苹果、生石榴等植物中.下列关于这两种有机化合物的说法正确的是( )| A. | 两种酸遇三氯化铁溶液都显色 | |
| B. | 鞣酸分子比莽草酸分子多两个双键 | |
| C. | 等物质的量的两种酸与NaOH反应,消耗NaOH的量相同 | |
| D. | 两种酸都能与溴水反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碱金属在空气中加热均可生成多种氧化物 | |
| B. | 碱金属与水反应,均浮在水面上. | |
| C. | 卤素各单质都能和水剧烈反应. | |
| D. | 卤素单质越活泼,其熔沸点就越低 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl-的结构示意图: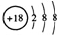 | |
| B. | 质子数为53,中子数为78的碘原子:${\;}_{53}^{131}$I | |
| C. | 光导纤维主要成分的化学式:Si | |
| D. | H216O、D216O、H218O、D218O互为同位素 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | x=10时,溶液中有NH4+、Al3+、SO42-,且c(NH4+)=c(Al3+) | |
| B. | x=20时,溶液中所发生的反应离子方程式为:Al3++2SO42-+2Ba2++4OH-═2BaSO4↓+AlO2-+2H2O | |
| C. | x=30时,溶液中有Ba2+、AlO2-、OH-,且c(OH-)>c(AlO2-) | |
| D. | 滴加过程中,生成沉淀的最大物质的量为0.003mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C3N4是分子晶体 | |
| B. | C3N4晶体中微粒通过离子键结合 | |
| C. | C3N4晶体具有导电性和延展性 | |
| D. | C3N4晶体是以C、N原子为基本微粒,共价键为作用力的空间网状结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将SO2气体通入NaClO溶液中:SO2+ClO-+H2O=SO32-+2HClO | |
| B. | 向FeBr2溶液中通入过量Cl2:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- | |
| C. | 三氯化铝溶液与足量的氨水反应:Al3++4OH-=[Al(OH)4]- | |
| D. | 用三氯化铁溶液腐蚀铜印刷电路板:2Fe3++Cu=Cu2++2Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 中性溶液中可能大量存在:Ca2+,Cl-,SO42-,K+ | |
| B. | 弱酸性溶液中可能大量存在:Cu2+,NH4+,NO3-,Cl- | |
| C. | 使石蕊试液变蓝的溶液中可能大量存在:Na+,Al3+,SO42-,NO3- | |
| D. | 水电离的c(OH-)=10-10mol/L溶液中可能大量存在:l-,NO3-,Mg2+,K+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com