
| A. | 其他条件不变时,升高温度,化学反应速率加快 | |
| B. | 其他条件不变时,增大浓度,化学反应速率加快 | |
| C. | 化学反应达到反应限度时,反应物的浓度与生成物的浓度相等 | |
| D. | 化学反应的限度是不可以改变的 |
科目:高中化学 来源: 题型:填空题
 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 编号 | ① | ② | ③ | ④ |
| 装置 |  |  |  |  |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属A在常温下能与浓硝酸反应,而B不能 | |
| B. | 金属A的阳离子的氧化性比金属B的阳离子的氧化性弱 | |
| C. | 工业上制取金属A只能用电解的方法,而金属B一般都用还原剂将其还原 | |
| D. | 将金属A和金属B用导线相连后插入某电解质溶液中构成原电池,金属A作负极 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 丙烷与氯气在光照条件下生成氯丙烷 | |
| B. | 乙烯与溴的四氯化碳溶液反应生成1,2二溴乙烷 | |
| C. | 乙烯与水反应生成乙醇 | |
| D. | 乙烯自身聚合生成聚乙烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 一段时间后,铁极质量会变大 | B. | 溶液中的H+向石墨电极移动 | ||
| C. | 电子由石墨电极通过导线流向铁极 | D. | 铁电极是该电池的正极 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | ||
| Y | ||
| Z |
| A. | Y元素原子的外围电子排布为4s24p4 | |
| B. | Y元素在周期表的第三周期第ⅥA族 | |
| C. | X元素所在周期中所含非金属元素最多 | |
| D. | Z元素原子的核外电子排布式为1s22s22p63s23p63d104s24p3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳氢原子个数比为1:3的烃有两种 | |
| B. | 碳碳间以单键结合,碳原子剩余价键全部与氢原子结合的烃一定是饱和链烃 | |
| C. | 丙烷分子中的3个碳原子一定在同一平面上,丁烷分子中的4个碳原子不一定 | |
| D. | 常温下,液态烷中仅有一种一氯代物的只有新戊烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
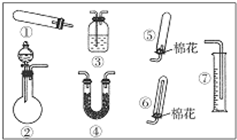 某同学用如图装置(固定、加热仪器和橡胶管略)进行有关氨气制取的实验探究.回答下列问题:
某同学用如图装置(固定、加热仪器和橡胶管略)进行有关氨气制取的实验探究.回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com