
【题目】某电动汽车使用的是高铁电池,其总反应为3Zn(OH)2+2Fe(OH)3+4KOH ![]() 3Zn+2K2FeO4+8H2O,下列说法正确的是( )
3Zn+2K2FeO4+8H2O,下列说法正确的是( )
A.放电时,若有6mol电子发生转移,则有2mol K2FeO4被氧化
B.放电时,正极反应为:FeO42﹣+4H2O+3e﹣═Fe(OH)3+5OH﹣
C.充电时,电池的负极与外接电源的正极相连
D.充电时,阴极附近溶液的pH变小
科目:高中化学 来源: 题型:
【题目】以硅孔雀石[主要成分为 CuCO3Cu(OH)2、CuSiO32H2O,含 SiO2、FeCO3、Fe2O3等杂质]为原料制备CuCl2的工艺流程如下: 
已知:SOCl2+H2O ![]() SO2↑+2HCl↑
SO2↑+2HCl↑
(1)“酸浸”时盐酸与CuCO3Cu(OH)2反应的化学方程式为 . 为提高“酸浸”时铜元素的浸出率,可以采取的措施有:①适当提高盐酸浓度;②适当提高反应温度;③ .
(2)滤渣2的主要成分为(填化学式).
(3)“氧化”时发生反应的离子方程式为 .
(4)试剂X的作用是调节溶液的PH,试剂X可以是
A.CuSO4 B.Cu2(OH)2CO3 C.NaOH D.CuO
“调pH”时,PH不能过高,其原因是 .
(5)“加热脱水”时,加入SOCl2的目的是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫及其化合物对人类的生产和生活有着重要的作用.
2SO2(g)+O2(g)2SO3(g)△H=﹣198kJmol﹣1是制备硫酸的重要反应.
(1)在容积为V L的密闭容器中起始充入2mol SO2和1mol O2 , 反应在不同条件下进行,反应体系总压强随时间的变化如下图所示.与实验a相比,实验b改变的条件是 , 判断的依据 . 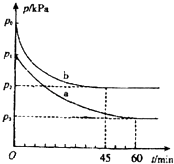
(2)二氧化硫在一定条件下还可以发生如下反应:
SO2(g)+NO2(g)SO3(g)+NO(g)△H=﹣42kJmol﹣1 .
在1L恒容密闭容器中充入SO2(g)和NO2(g),所得实验数据如下:
实验编号 | 温度 | 起始时物质的量/mol | 平衡时物质的量/mol | |
N(SO2) | N(NO2) | N(NO) | ||
甲 | T1 | 0.80 | 0.20 | 0.18 |
乙 | T2 | 0.20 | 0.80 | 0.16 |
丙 | T3 | 0.20 | 0.30 | a |
①实验甲中,若2min时测得放出的热量是4.2kJ,则0~2min时间内,用SO2(g)表示的平均反应速率v(SO2)= , 该温度下的平衡常数 .
②实验丙中,达到平衡时,NO2的转化率为 .
③由表中数据可推知,TlT2(填“>”“<’’或“=”),判断的理由是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】己烯雌酚是一种激素类药物,结构如图所示,下列有关叙述中正确的是( ) 
A.该有机物属于芳香烃
B.该物质不能使酸性高锰酸钾溶液褪色
C.该分子对称性好,所以没有顺反异构
D.该有机物分子中,最多可能有18个碳原子共平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】运用盖斯定律可方便地计算出难以通过实验直接测定的反应热。
已知:①P4(白磷,s)+5O2(g)![]() P4O10(s) ΔH=2 983.2 kJ·mol1
P4O10(s) ΔH=2 983.2 kJ·mol1
②P(红磷,s)+![]() O2(g)
O2(g)![]()
![]() P4O10(s) ΔH=738.5 kJ·mol1
P4O10(s) ΔH=738.5 kJ·mol1
则白磷转化为红磷的热化学方程式为
A.P4(白磷,s)![]() 4P(红磷,s) ΔH=29.2 kJ·mol1
4P(红磷,s) ΔH=29.2 kJ·mol1
B.P4(白磷,s)![]() 4P(红磷,s) ΔH=+29.2 kJ·mol1
4P(红磷,s) ΔH=+29.2 kJ·mol1
C.P4(白磷,s)![]() 4P(红磷,s) ΔH=2 244.7 kJ·mol1
4P(红磷,s) ΔH=2 244.7 kJ·mol1
D.P4(白磷,s)![]() 4P(红磷,s) ΔH=+2244.7 kJ·mol1
4P(红磷,s) ΔH=+2244.7 kJ·mol1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如图所示装置除去含有CN﹣、Cl﹣ 废水中的CN﹣时,控制溶液pH为9~10,阳极产生的ClO﹣将CN﹣氧化为两种无污染的气体,下列说法不正确的是( ) 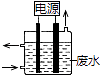
A.用石墨作阳极,铁作阴极
B.阳极的电极反应式:Cl﹣+2OH﹣﹣2e﹣═ClO﹣+H2O
C.阴极的电极反应式:2H2O+2e﹣═H2↑+2OH﹣
D.除去CN﹣的反应:2CN﹣+5ClO﹣+2H+═N2↑+2CO2↑+5Cl﹣+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知甲、乙、丙、丁都是含碳物质。其中丁是一种有机物,甲、乙、丁都能发生燃烧生成丙,同时放出大量的热,甲与丙反应时需要吸收热量。则甲、乙、丙、丁分别是 ( )
A.CO,C,CO2,CH4B.C,CO2,CH4,CO
C.C,CO,CO2,CH4D.C,O2,CO2,CH4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子组在指定溶液中能大量共存的是( )
A.强酸溶液中:K+、Fe2+、MnO4﹣、SO42﹣
B.![]() =0.1mol/L的溶液:Na+、K+、SiO32﹣、NO3﹣
=0.1mol/L的溶液:Na+、K+、SiO32﹣、NO3﹣
C.既能溶解Al(OH)3又能溶解 H2SiO3的溶液中:Na +、CO32﹣、SO32﹣、NO3﹣
D.在含有大量HCO3﹣的溶液中:K+、Na+、AlO2﹣、Br﹣
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com