
下列有关材料的说法不正确的是( )
A.传统的无机非金属材料虽然有不少优点,但质脆,经不起热冲击
B.新型无机非金属材料虽然克服了传统无机非金属材料的缺点,但强度比较差
C.高温结构材料具有能经受高温,不怕氧化,耐酸碱腐蚀,硬度大,耐磨损,密度小的优点
D.新型无机非金属材料特征之一是具有电学特性
科目:高中化学 来源: 题型:
已知反应X+Y= M+N为吸热反应,对这个反应的下列说法中正确的是
A.X的能量一定低于M的,Y的能量一定低于N的
B.因为该反应为吸热反应,故一定要加热反应才能进行
C.破坏反应物中的化学键所吸收的能量小于形成生成物中化学键所放出的能量
D.X和Y的总能量一定低于M和N的总能量
查看答案和解析>>
科目:高中化学 来源: 题型:
研究和深度开发CO、CO2的应用对构建生态文明社会具有重要的意义。
(1)CO可用于炼铁,已知:Fe2O3(s)+3C(s)=2Fe (s)+3CO(g) ΔH 1=+489.0 kJ· mol-1,
C(s) +CO2(g)=2CO(g) ΔH 2 =+172.5 kJ·mol-1, 则CO还原Fe2O3(s)的热化学方程式为 。
(2)CO与O2设计成燃料电池(以KOH溶液为电解液)。该电池的负极反应式为 。
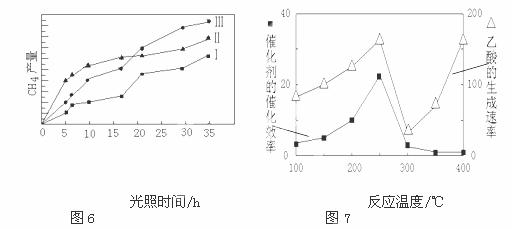
(3)CO2和H2充入一定体积的恒容密闭容器中,在两种温度下发生反应:CO2(g) +3H2(g) 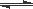 CH3OH(g) +H2O(g) 测得CH3OH的物质的量随时间的变化如图5。
CH3OH(g) +H2O(g) 测得CH3OH的物质的量随时间的变化如图5。
|

①该反应的ΔH 0(填“大于或小于”),曲线I、Ⅱ对应的平衡常数大小关系为
KⅠ KⅡ (填“>、=或<”)。
②一定温度下,在容积相同且固定的两个密闭容器中,按如下方式加入反应物,一段时间后达到平衡。
| 容 器 | 甲 | 乙 |
| 反应物投入量 | 1 mol CO2、3 mol H2 | a molCO2、3a molH2、 b molCH3OH(g)、b molH2O(g) |
若甲中平衡后气体的压强为开始的0.8倍,要使平衡后乙与甲中相同组分的体积分数相等,且起始时维持化学反应向逆反应方向进行,则b的取值范围为 。
(4)利用光能和光催化剂,可将CO2和H2O(g)转化为CH4和O2。紫外光照射时,在不同催化剂(I、II、III)作用下,CH4产量随光照时间的变化如图6。在0~15小时内,CH4的平均生成速率I、II和III从小到大的顺序为 (填序号)。
(5)以TiO2/Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成乙酸。
在不同温度下催化剂的催化效率与乙酸的生成速率的关系如图7。
①当温度在 范围时,温度是乙酸生成速率的主要影响因素。
②Cu2Al2O4可溶于稀硝酸,稀硝酸还原产物为NO,写出有关的离子方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列除去杂质的方法正确的是( )
①除去乙烷中少量的乙烯:光照条件下通入Cl2,气液分离
②除去乙酸乙酯中少量的乙酸:用饱和碳酸氢钠溶液洗涤、分液、干燥、蒸馏 ③除去CO2中少量的SO2:气体通过盛有饱和Na2CO3溶液的洗气瓶 ④除去乙醇中少量的乙酸:加足量的生石灰,蒸馏
A.①② B.②④
C.③④ D.②③
查看答案和解析>>
科目:高中化学 来源: 题型:
用下列提供的试剂和操作除去各种粉末状混合物中的杂质(括号内为杂质),将序号填在表格内,发生化学反应的写出其反应的化学方程式。
试剂:A.盐酸 B.烧碱溶液 C.氧气 D.水 E.二氧化碳 F.不加其他试剂
操作:(1)加热 (2)加热熔融 (3)高温灼烧 (4)过滤
(5)分液 (6)结晶
| 物质 | 试剂 | 操作 | 有关的化学方程式 |
| ①SiO2(CaCO3) | |||
| ②SiO2(Si) | |||
| ③NaCl(SiO2) | |||
| ④SiO2(NH4Cl) | |||
| ⑤Fe2O3(SiO2) |
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA代表阿伏加德罗常数,下列说法中正确的是( )
A.2.9 g 2CaSO4·H2O中含有的结晶水分子数为0.02NA
B.30 g乙酸和葡萄糖的混合物中含碳原子数为NA
C.在铁与硫的反应中,1 mol铁失去的电子数为3NA
D.62 g Na2O溶于水后所得溶液中含有的O2-数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
在平衡:2CrO42-(黄色)+2H+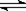 Cr2O72-(橙红色)+H2O中,溶液颜色介于黄色和橙红色之间。若使溶液的橙红色加深,则应向溶液中加入的是
Cr2O72-(橙红色)+H2O中,溶液颜色介于黄色和橙红色之间。若使溶液的橙红色加深,则应向溶液中加入的是
A.少量浓硫酸 B.少量氢氧化钠固体 C.少量氯化钾固体 D.少量H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
下列化学反应的离子方程式正确的是 ( )
A.钢铁发生吸氧腐蚀时,铁作负极被氧化:Fe-3e-=Fe3+
B.铁溶于稀硝酸,溶液变黄:3Fe +8H+ +2NO3-=3Fe2++2NO↑+4H2O
C.向NaAlO2溶液中通入过量的CO2:CO2+ 2AlO2- + 3H2O =2Al(OH)3 ↓ + CO32-
D.用小苏打治疗胃酸过多:HCO3-+H+ = CO2↑+H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com