
【题目】钚(23994Pu)是制造威力更大原子弹的良好原料。下列有关说法错误的是
A. 原子序数为94 B. 电子数为94 C. 中子数为94 D. 质量数为239
科目:高中化学 来源: 题型:
【题目】在三个容积均为1L的恒温恒容密闭容器中,起始时按表中相应的量加入物质,在相同温度下发生反应3CO(g)+3H2(g)![]() (CH3)2O(g)+CO2(g)(不发生其他反应),CO的平衡转化率与温度和压强的关系加下图所示。
(CH3)2O(g)+CO2(g)(不发生其他反应),CO的平衡转化率与温度和压强的关系加下图所示。
容器 | 起始物质的量/mol | 平衡 转化率 | |||
CO | H2 | (CH3)2O | CO2 | CO | |
Ⅰ | 0.3 | 0.3 | 0 | 0 | 50% |
Ⅱ | 0.3 | 0.3 | 0 | 0.1 | |
Ⅲ | 0 | 0 | 0.2 | 0.4 | |

下列说法正确的是( )
A. 该反应的△H<0,图中压强p1>p2
B. 达到平衡时,容器Ⅱ中CO的平衡转化率大于50%
C. 达到平衡时,容器Ⅰ与容器Ⅱ的总压强之比小于4∶5
D. 达到平衡时,容器Ⅲ中n[(CH3)2O]是容器Ⅱ中的2倍
查看答案和解析>>
科目:高中化学 来源: 题型:
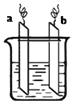
【题目】下图,两电极上发生的电极反应分别为:a极:Ag++e-=Ag b极:Fe-2e-=Fe2+
下列说法正确的是( )
A. a极材料一定为金属银
B. b极一定连电源的正极
C. 装置中电解质溶液阳离子一定只含有Ag+
D. 装置中发生的反应方程式一定是Fe +2Ag+===Fe2++2Ag
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硒是制造光电池的一种原料,人体缺少硒就会得“克山病”。从电解精炼铜的阳极泥中提取硒的流程如下,已知阳极泥中硒以Se、Ag2Se、Cu2Se等形式存在:

请回答下列问题:
(1)电解精炼铜时,粗铜与电源的_____(填“正极”或“负极”)相连。
(2)SeO2溶于水得到H2SeO3(Ka1=3.5×10-3,Ka2=5.0×10-8),常温下亚硒酸溶液与少量氢氧化钠溶液反应的离子方程式为:_________________,反应所得的盐形成的溶液pH____7,(填>、<或=)原因是________________________________(用相关数据及必要的文字说明)
(3)亚硒酸溶液与SO2反应制硒的化学方程式为_____________________________。电解亚硒酸溶液可制得强酸H2SeO4,则电解时的阴极反应式为________________。
(4)上述硒的提取过程中除了焙烧过程中浓硫酸有强烈的腐蚀性外,还存在的主要问题是___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 将苯加入溴水中振荡后,水层接近无色,是因为发生了取代反应
B. 2,2-二甲基丙烷也称新戊烷
C. 等质量的乙烯和乙醇在氧气中充分燃烧耗氧量相同
D. 环己醇能与氢氧化钠溶液反应且所有碳原子可以共面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应3Cl2+6NaOH![]() 5NaCl+NaClO3+3H2O,以下叙述正确的是( )
5NaCl+NaClO3+3H2O,以下叙述正确的是( )
A. Cl2既做氧化剂又做还原剂
B. 被氧化的氯原子和被还原的氯原子的物质的量之比为5∶1
C. Cl2是氧化剂,NaOH是还原剂
D. 氧化剂得电子数与还原剂失电子数之比为5∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四川师范大学化学与材料学院对“铁与水蒸气反应”实验研究的结果显示:在80~100℃能产生稳定水蒸气的物质都可以作为该反应的供水剂;铁与水蒸气反应温度在500℃左右即可顺利进行。
某化学兴趣小组同学利用该研究结论,采用西红柿(或洋葱)作为供水剂,设计了如图装置进行实验,并对铁与水蒸气反应的产物进行检验。

回答下列问题:
(1)A中铁与水蒸气反应的化学方程式是_______________。
(2)C中碱石灰的作用是______________。
(3)D处实验现象为___________________________。
(4)上述实验结束后,取出A中铁粉反应后的少量固体继续进行如下实验:

①加入稀硫酸发生的离子方程式为______________________________。
②试剂A是_____________(选填字母),现象2为___________________。
a .NaOH溶液 b. 酸性KMnO4溶液 c .酚酞 d . 氯水
③若用电子天平称取铁粉质量为0.1527g,测得生成氢气体积为73.50mL(实验室条件下气体摩尔体积为24.5L/mol).则参加反应的铁粉占称取铁粉的百分数为_____(精确到0.1%)。
④有同学认为:即使得到了现象1和现象2的实验现象,也不能确定所得固体成分为Fe3O4。你认为该同学持此看法的理由是_______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com