
【题目】一定条件下反应N2(g)+3H2(g) ![]() 2NH3(g )在10L的密闭容器中进行,测得2min内,N2的物质的量由20mol减小到8mol,则2min内NH3的反应速率为
2NH3(g )在10L的密闭容器中进行,测得2min内,N2的物质的量由20mol减小到8mol,则2min内NH3的反应速率为
A.1.2mol/(L·min)B.1.8mol/(L·min)
C.0.6mol/(L·min)D.0.4mol/(L·min)
 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】NaC1O3可用于制取二氧化氯、亚氯酸钠及高氯酸盐等。以原盐(主要成分为NaC1)为原料制备氯酸钠的工艺流程如下:

已知:Cr2O72-+H2O![]() 2CrO42-+2H+。
2CrO42-+2H+。
回答下列问题:
(1)“粗制盐水”中加入NaOH和Na2CO3的目的是___________________。
(2)过滤时,使用的玻璃仪器有烧杯、玻璃棒和____________。
(3)在pH:6.4~6.8,温度:40~50℃的条件下电解,理论上最终产物只有NaC1O3。电解时阳极的产物为C12,溶液中发生的反应有C12+H2O====HC1O+H++C1-,HC1O![]() H++C1O-和__________。
H++C1O-和__________。
(4)电解槽中温度不宜过高,其原因是_________________________。加入的Na2Cr2O7可以调节电解液酸度,若酸度过大,则电解液中主要存在__________(填“Cr2O72-”或“CrO42-”)。
(5)为检测电解后盐水中NaC1O3的物质的量浓度进行下列实验:
I.准确吸取10.00mL电解后的盐水,加入适量的3%H2O2溶液充分搅拌并煮沸。
Ⅱ.准确吸取0.10mol·L-1的(NH4)2Fe(SO4)2标准溶液25.00 mL于300mL锥形瓶中,加入足量稀硫酸。
III.将I的溶液加入Ⅱ的锥形瓶中,隔绝空气煮沸10min,加热充分反应。冷却至室温后,加入10mL0.4mol·L-1MnSO4溶液、5mL 85%磷酸溶液,用c mol·L-1的KMnO4标准溶液滴定剩余的Fe2+至溶液变为微红色,即滴定终点,此时消耗高锰酸钾V mL。
①步骤I中加入H2O2溶液的作用是______________________。
②步骤Ⅱ中C1O3-被Fe2+还原为C1-的离子方程式为________________________。
③该盐水中NaC1O3的物质的量浓度为________mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D四种元素,A元素的原子得两个电子,B元素的原子失去1个电子后所形成微粒均与氩原子有相同的电子层结构。C元素的原子只有1个电子,D元素原子的M电子层数比N层电子数多6个。试写出:
(1)A、B、C、D的元素符号和名称:A____ B____C____D____。
(2)A元素的原子结构示意图____,D元素的离子结构示意图:______。
(3)画出A离子的电子式____B原子的电子式____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从2011年3月1日起,欧盟禁止生产含双酚A的塑料奶瓶。工业上双酚A系由苯酚和丙酮在酸性介质中制得: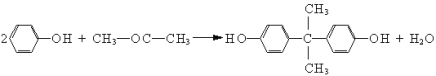 。下列说法中正确的是
。下列说法中正确的是
A. 该反应属于加成反应
B. 苯酚和双酚A都可以与NaHCO3反应
C. 苯酚有毒,但稀的苯酚溶液可用于杀菌消毒
D. 1mol苯酚和1mol双酚A最多都可以与3mol溴发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下用NaOH溶液滴定H2C2O4溶液溶液中﹣lg![]() 和﹣lgc(HC2O4-)[或-lg
和﹣lgc(HC2O4-)[或-lg![]() 和﹣lgc(C2O42-)]的关系如图所示。下列说法正确的是( )
和﹣lgc(C2O42-)]的关系如图所示。下列说法正确的是( )

A. 曲线N表示-lg![]() 和﹣lgc(C2O42-)的关系
和﹣lgc(C2O42-)的关系
B. Ka1(H2C2O4)的数量级为10﹣1
C. 向NaHC2O4溶液中加少量NaOH至c(HC2O4﹣)和c(C2O42﹣)相等,此时溶液pH约为4
D. 在Na2C2O4和NaHC2O4物质的量为1:1的混合溶液中c(Na+)>c(C2O42﹣)>c(HC2O4﹣)>c(H2C2O4)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】写出下列有机反应的化学方程式:
(1)用乙炔为原料制备聚氯乙烯(两个反应):______;______。
(2)向苯酚浊液中加入少量氢氧化钠,溶液变澄清;再通入CO2,溶液又变浑浊(两个反应):_____;____。
(3)乙二酸和乙二醇反应生成六元环酯:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下的a L H2和Cl2的混合气体,经光照充分反应后,所得气体恰好使溶液中b molNaOH完全转变为盐,则a、b的关系不可能是
A.b=a/22.4B.0<b<a/22.4C.b>a/22.4D.b≥a/11.2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】C、N、S的氧化物常会造成一些环境问题,科研工作者正在研究用各种化学方法来消除这些物质对环境的不利影响。
(1)尿素[CO(NH2)2]是一种非常重要的高效氮肥,工业上以NH3、CO2为原料生产尿素,该反应实际为两步反应:
第一步:2NH3(g)+CO2(g) ![]() H2NCOONH4(s) △H=-272KJ·mol-1
H2NCOONH4(s) △H=-272KJ·mol-1
第二步:H2NCOONH4(s) ![]() CO(NH2)2(s)+H2O(g) △H=+138kJ·mol-1
CO(NH2)2(s)+H2O(g) △H=+138kJ·mol-1
写出工业上以NH3、CO2为原料合成尿素的热化学方程式:______________________。
(2)一定温度下,向2L恒容密闭容器中通入2molCO和1mol SO2,发生反应2CO(g)+SO2(g) ![]() 2CO2(g)+S(s)。若反应进行到20min时达平衡,测得CO2的体积分数为0.5,则前20min的反应速率v(CO)=_________,该温度下反应化学平衡常数K=__________。
2CO2(g)+S(s)。若反应进行到20min时达平衡,测得CO2的体积分数为0.5,则前20min的反应速率v(CO)=_________,该温度下反应化学平衡常数K=__________。

(3)工业上可用NaC1O碱性溶液或“亚硫酸盐法”吸收SO2。
①为了提高吸收效率,常用Ni2O3作为催化剂。催化过程如图所示:
a.过程2的离子方程式_______________________________。
b.Ca(C1O)2也可用于脱硫,且脱硫效果比NaC1O更好,原因是________________。
②室温条件下,将烟气通入(NH4)2SO4溶液中,测得溶液pH与含硫组分物质的量分数的变化关系如图所示,b点时溶液pH=7,则n(NH4+):n(SO32-)=__________。
(4)用食盐水做电解液电解烟气脱氮的原理如图,NO被阳极产生的氧化性物质氧化为NO3-,尾气经氢氧化钠溶液吸收后排入空气。如下图,电流密度和溶液pH对烟气脱硝的影响。

①NO被阳极产生的氧化性物质氧化为NO3-反应的离子方程式___________________。
②溶液的pH对NO去除率影响的原因是______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com