
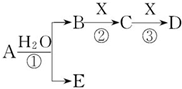
 A、B、C、D、E是短周期元素组成的中学常见的物质,它们的转化关系如图所示(部分产物和反应条件略去):
A、B、C、D、E是短周期元素组成的中学常见的物质,它们的转化关系如图所示(部分产物和反应条件略去):| 2.4mol |
| 2L |
| 0.15mol |
| 2L |
| 0.6mol |
| 2L |
| 0.3×0.3 |
| 1.2×0.075 |
| 3x×3x |
| 3(1-x).(4.5-3x) |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、直径介于1nm~100nm之间的微粒称为胶体 |
| B、电泳现象可证明胶体带电 |
| C、可用丁达尔效应来区分溶液和胶体 |
| D、刚含1molFeCl3的溶液可制得6.02×1023个Fe(OH)3胶体粒子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、互为同位素 |
| B、都属于镧系元素 |
| C、中子数相等 |
| D、原子质量几乎相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 催化剂 |
| △ |
| 时间min | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 |
| n(SO2) | 2.00 | 1.92 | 1.84 | 1.76 | 1.76 | 1.64 | 1.52 | 1.40 | 1.40 | 1.40 |
| n(O2) | 1.00 | 0.96 | 0.92 | 0.88 | 0.88 | 0.82 | 0.76 | 0.70 | 0.70 | 0.70 |
| n(SO3) | 0 | 0.08 | 0.16 | 0.24 | 0.24 | 0.36 | 0.48 | 0.60 | 0.60 | 0.60 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、反应开始至2分钟时,以B浓度变化表示的反应速率为0.05mol/(L?min) |
| B、反应开始至2分钟时,A的转化率为10% |
| C、若其他条件不变,升高温度,A的体积分数增大,则该反应的△H<0 |
D、若其他条件不变,增大压强,化学反应速率的变化符合右侧示意图 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com