
通过下列方法可以测定金属锡的纯度:
①将试样溶于盐酸中,发生的反应为:Sn+2HCl=SnCl2+H2↑
②加入过量的FeCl3溶液,发生的反应为:SnCl2+2FeCl3=SnCl4+2FeCl2
③用已知浓度的K2Cr2O7溶液滴定生成的Fe2+,发生的反应为:
6FeCl2+K2Cr2O7+14HCl=6FeCl3+2KCl+2CrCl3+7H2O
(1)上述氧化还原反应中,HCl作氧化剂的是________(填“①”、“②”或“③”).
(2)现有金属锡样品0.613 g,经上述各步反应后,共用去0.100 mol/L K2Cr2O7溶液16.0 mL.求试样中锡的质量分数(假设杂质不参加反应).
科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
 白质含量,导致许多婴幼儿肾结石.
白质含量,导致许多婴幼儿肾结石.








| 反应物 |
| 反应条件 |
| 反应物 |
| 反应条件 |


查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
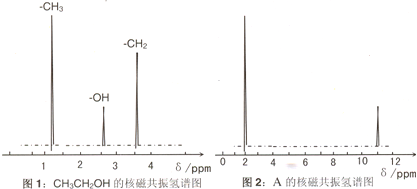
查看答案和解析>>
科目:高中化学 来源:2013-2014学年安徽省“江南十校”高三3月联考理综化学试卷(解析版) 题型:填空题
硫酸亚锡(SnSO4)是一种重要的能溶于水的硫酸盐,广泛应用于镀锡工业。某研究小组
设计SnSO4制备路线如下:
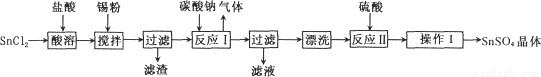
查阅资料:
I.酸性条件下,锡在水溶液中有Sn2+、Sn4+两种主要存在形式,Sn2+易被氧化。
Ⅱ.SnC12易水解生成碱式氯化亚锡[Sn(OH)Cl]
回答下列问题:
(1)操作l的步骤为 ____、____、过滤、洗涤、干燥。对沉淀进行洗涤的方法是_____________。
(2) SnCl2粉末需加浓盐酸进行溶解,请结合必要的化学方程式用平衡移动原理解释原因:________。
(3)加入Sn粉的作用有两个:①调节溶液pH;②__________。
(4)酸性条件下,SnSO4还可以用作双氧水去除剂,发生反应的离子方程式是:________________。
(5)该小组通过下列方法测定所用锡粉的纯度(杂质不参与反应):取ag锡粉溶于盐酸中,向生成的SnC12中加入过量的FeC13溶液,用b mol/LK2Cr2O7滴定生成的Fe2+(已知酸性环境下,Cr2O72-可被还原为Cr3+),共用去K2Cr2O7溶液m ml。则锡粉中锡的质量分数是________。(Sn的摩尔质量为M g/mol,用含a、b、m、M的代数式表示)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com