
| A、标准状况下,22.4 L水中含有的水分子数是NA |
| B、0.10mol?L-1NaCl溶液中含有Cl-离子数是0.1NA |
| C、NA个O2分子的质量是16g |
| D、N=n?NA |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A | B | C | D | |
| X | 酸 | 碱性氧化物 | 盐 | 羧酸 |
| Y | 碱 | 酸 | 碱 | 醇 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1:2 | B、1:4 |
| C、大于1:4 | D、小于1:4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钢铁发生吸氧腐蚀时的正极反应:O2+4e-+4H+═2H2O |
| B、小苏打水解反应的离子方程式:HCO3-+H2O?CO32-+H3O+ |
| C、氯碱工业和工业冶炼金属钠的阳极反应均为:2Cl--2e-═Cl2↑ |
| D、NaAlO2溶液中通入足量CO2的离子方程式:2AlO2-+CO2+3H2O═2Al(OH)3↓+CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
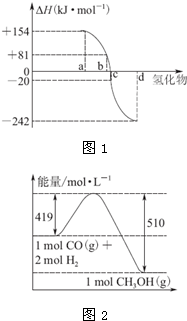 热力学标准态(298K、101kPa)下,由稳定单质发生反应生成1mol 化合物的反应热叫该化合物的生成热(△H).
热力学标准态(298K、101kPa)下,由稳定单质发生反应生成1mol 化合物的反应热叫该化合物的生成热(△H).| 800℃、Ar |
| Mg |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com