
有些科学家提出硅是“21世纪的能源”,这主要是由于作为半导体材料的硅在太阳能发电过程中具有重要的作用。下列有关硅的说法中,不正确的是 ( )
A.高纯度的硅广泛用于制作计算机芯片
B.硅可由二氧化硅还原制得
C.低温时,硅与水、空气和酸不反应,但能与氢氟酸反应
D.自然界中硅的储量丰富,自然界中存在大量的单质硅
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案 口算心算速算应用题系列答案
口算心算速算应用题系列答案科目:高中化学 来源: 题型:
随着人们生活节奏的加快,方便的小包装食品已被广泛接受。为了延长食品的保
质期,防止食品氧化变质,在包装袋中可以放入的化学物质是
 A.无水硫酸铜 B.硫酸亚铁 C. 食盐 D. 生石灰
A.无水硫酸铜 B.硫酸亚铁 C. 食盐 D. 生石灰
查看答案和解析>>
科目:高中化学 来源: 题型:
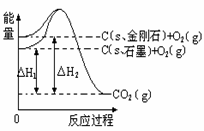
如下图所示,△H1=-393.5 kJ?mol-1,
△H2=-395.4 kJ?mol-1,下列说法或表示式正确的是
A. C(s、石墨)== C(s、金刚石) △H= - 1.9 kJ?mol-1
B. 石墨和金刚石的转化是物理变化
C. 石墨的稳定性强于金刚石
D. 1 mol石墨的总键能比1 mol金刚石的总键能小1.9 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
用四种溶液进行实验,下表中“操作及现象”与“溶液”对应关系错误的是 ( )
| 选项 | 操作及现象 | 溶液 |
| A | 通入CO2,溶液变浑浊 | 饱和Na2CO3溶液 |
| B | 通入CO2,溶液变浑浊,继续通CO2至过量,浑浊消失 | Na2SiO3溶液 |
| C | 通入CO2,溶液变浑浊,再加入品红溶液,红色褪去 | Ca(ClO)2溶液 |
| D | 通入CO2,溶液变浑浊,继续通CO2至过量,浑浊消失,再加入足量NaOH溶液,又变浑浊 | 澄清石灰水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
判断正误,正确的划“√”,错误的划“×”
(1)单质硅是将太阳能转变为电能的常用材料 ( )
(2012·新课标全国卷,8B)
(2)合成纤维和光导纤维都是新型无机非金属材料 ( )
(2012·新课标全国卷,8D)
(3)甲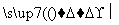 乙
乙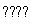 丙,若甲为焦炭,则丁可能是O2 ( )
丙,若甲为焦炭,则丁可能是O2 ( )
(2013·江苏,6A)
(4)SiO2可与HF反应,因而氢氟酸不能保存在玻璃瓶中 ( )
(2013·广东理综,10D)
(5)高温下用焦炭还原SiO2制取粗硅 ( )
(2013·广东理综,11C)
(6)SiO2有导电性,所以SiO2可用于制备光导纤维 ( )
(2012·广东理综,12B)
(7)硅酸钠溶液应保存在带玻璃塞的试剂瓶中 ( )
(2012·海南,4B)
(8)水玻璃可用于生产黏合剂和防火剂 ( )
(2010·江苏,4B)
查看答案和解析>>
科目:高中化学 来源: 题型:
将足量CO2气体通入水玻璃(Na2SiO3溶液)中,然后加热蒸干,再在高温下充分灼烧,最后得到的固体物质是 ( )
A.Na2SiO3 B.Na2CO3、Na2SiO3
C.Na2CO3、SiO2 D.SiO2
查看答案和解析>>
科目:高中化学 来源: 题型:
氮化硅(Si3N4)是一种优良的高温结构陶瓷,在工业生产和科技领域中有重要用途。
Ⅰ.工业上有多种方法来制备氮化硅,下面是几种常见的方法:
方法一 直接氮化法:在1 300~1 400 ℃时,高纯粉状硅与纯氮气化合,其反应方程式为________________________________________________________________________。
方法二 化学气相沉积法:在高温条件下利用四氯化硅气体、纯氮气、氢气反应生成氮化硅和HCl,与方法一相比,用此法制得的氮化硅纯度较高,其原因是________________________________________________________________________。
方法三 Si(NH2)4热分解法:先用四氯化硅与氨气反应生成Si(NH2)4和一种气体________________(填分子式);然后使Si(NH2)4受热分解,分解后的另一种产物的分子式为____________________。
Ⅱ.(1)氮化硅抗腐蚀能力很强,但易被氢氟酸腐蚀,氮化硅与氢氟酸反应生成四氟化硅和一种铵盐,此盐中存在的化学键类型有______________。
(2)已知:25 ℃,101 kPa条件下的热化学方程式:
3Si(s)+2N2(g)===Si3N4(s) ΔH=-750.2 kJ·mol-1①
Si(s)+2Cl2(g)===SiCl4(g) ΔH=-609.6 kJ·mol-1②
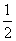 H2(g)+
H2(g)+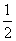 Cl2(g)===HCl(g) ΔH=-92.3 kJ·mol-1③
Cl2(g)===HCl(g) ΔH=-92.3 kJ·mol-1③
请写出四氯化硅气体与氮气、氢气反应的热化学方程式:
________________________________________________________________________。
Ⅲ.工业上制取高纯硅和四氯化硅的生产流程如下:

已知:X、高纯硅、原料B的主要成分都可与Z反应,Y与X在光照或点燃条件下可反应,Z的焰色呈黄色。
(1)原料B的主要成分是________(写名称)。
(2)写出焦炭与原料B中的主要成分反应的化学方程式:
________________________________________________________________________。
(3)上述生产流程中电解A的水溶液时,阳极材料能否用Cu?________(填“能”或“不能”)。写出Cu为阳极电解A的水溶液开始一段时间阴、阳极的电极方程式。
阳极:________;阴极________。
查看答案和解析>>
科目:高中化学 来源: 题型:
向含有Mn2+的酸性溶液中滴加过二硫酸钾(K2S2O8)溶液,会发生如下反应(未配平):Mn2++S2O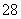 +H2O―→MnO
+H2O―→MnO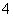 +SO
+SO +H+。下列说法正确的是( )
+H+。下列说法正确的是( )
A.该反应中起氧化作用的是Mn2+
B.反应后溶液的pH降低
C.反应中有1 mol还原剂参加反应,则转移的电子为4 mol
D.该反应常用于检验溶液中Mn2+的存在,现象是溶液紫红色消失
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是 ( )
①氯气的性质活泼,它与氢气混合后立即发生爆炸 ②实验室制取氯气时,为了防止环境污染,多余的氯气可以用氢氧化钙溶液吸收 ③新制氯水的氧化性强于久置氯水的
④检验HCl气体中是否混有Cl2,方法是将气体通入硝酸银溶液 ⑤除去HCl气体中的Cl2,可将气体通入饱和食盐水中
A.①②③ B.②③④ C.③ D.③⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com