
【题目】工业上制取高纯度硅的反应之一为SiCl4+2H2![]() Si+4HCl。该反应属于( )
Si+4HCl。该反应属于( )
A. 化合反应B. 分解反应
C. 置换反应D. 复分解反应
科目:高中化学 来源: 题型:
【题目】已知某校回收的含银悬浊废水中含有AgCl、Ag(NH3)2NO3、AgNO3、CH3COONH4、NaCl等,设计从废水中回收硝酸银的具体流程如下:
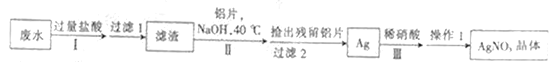
下列说法不正确的是
A. 步骤Ⅱ中发生的主要反应的离子方程:3AgCl+Al+4OH-=3Ag+AlO2-+3Cl-+2H2O
B. 实验中用铝粉代替铝片可以加快反应速率并简化实验操作
C. 步骤Ⅲ中若先将Ag氧化为Ag2O,再加入稀硝酸反应有利于环保
D. 操作Ⅰ包括蒸发浓缩、冷却结晶、过滤、洗涤等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验误差分析错误的是( )
A.用容量瓶配制溶液,定容时俯视刻度线,所配溶液浓度偏小
B.排水量气,左右液面相平后,未冷却到室温立即读数,所得气体的体积偏大
C.称取2.3gNaCl固体,砝码放在托盘天平的左边,所称量固体药品质量偏小
D.用量筒量取5.0mL浓硫酸,仰视读数,所得到浓硫酸的体积偏大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示甲、乙两个装置,所盛溶液体积和浓度均相同且足量,电极铝和镁都已除去表面氧化膜。当两装置电路中通过的电子都是1mol时,下列说法不正确的是
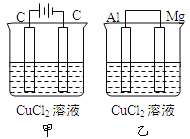
A. 溶液的质量减小程度:乙<甲
B. 溶液的导电能力变化:甲>乙
C. 甲中阴极和乙中镁电极上析出物质质量:甲=乙
D. 电极反应式:甲中阳极:![]() -2e → Cl2↑,乙中正极:
-2e → Cl2↑,乙中正极:![]() + 2e → Cu
+ 2e → Cu
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高纯度氧化铝有广泛的用途,某研究小组研究用以下流程制取高纯度氧化铝:
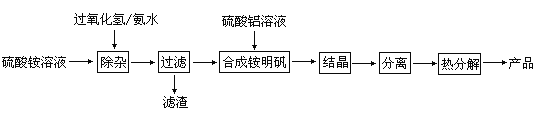
根据上述流程图填空:
(1)“除杂”操作是加入过氧化氢后,用氨水调节溶液的pH约为8.0,以除去硫酸铵溶液中的少量Fe2+。请写出在除去Fe2+离子的过程中,发生的主要反应的离子方程式____________________________。
(2)通常条件下Ksp〔Fe(OH)3〕=4.0×10—38,除杂后溶液中c(Fe3+)约为_____________。
(3)配制硫酸铝溶液时,需用硫酸酸化,酸化的目的是________________________。
(4)“结晶”这步操作中,母液经蒸发浓缩至溶液表面刚出现薄层晶体即停止加热,然后冷却结晶,得到铵明矾晶体(含结晶水)。母液不能蒸干的原因是____________。
(5)“分离”操作的名称是_____________(填字母代号)。
A.蒸馏 B.分液 C.过滤
(6)铵明矾晶体的化学式为NH4Al(SO4)2·12H2O,在0.1mol/L铵明矾的水溶液中,离子浓度最大的离子是__________,离子浓度最小的离子是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属钠是在1807年通过电解氢氧化钠制得的,这个原理应用于工业生产,约在1891年才获得成功。1921年实现了电解氯化钠制钠的工业方法,其反应原理是:2NaCl(熔融)![]() 2Na+Cl2↑。回答下列有关单质钠的问题:
2Na+Cl2↑。回答下列有关单质钠的问题:
(1)下列各项中属于保存金属钠的正确方法是____。
A.放在棕色瓶中 B.放在细沙中
C.放在水中 D.放在煤油中
(2)钠长时间放在空气中,最后的产物主要成分是____。
A.Na2O B.Na2O2 C.NaOH D.Na2CO3
(3)将一小块钠放在水平放置的试管中部,用酒精灯加热充分反应(如图Ⅰ所示),请写出该反应的化学方程式____________,生成物的颜色为____。将该试管冷却后直立,滴加几滴水(如图Ⅱ所示),发生反应的化学方程式为____________,检验该反应产生的气体的方法是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将2 mol SO2和1 mol O2充入一容积固定的密闭容器中,在一定条件下发生反应:2SO2(g)+O2(g) ![]() 2SO3(g),下列物理量不再改变时,并不能说明化学反应已达到平衡状态的是( )
2SO3(g),下列物理量不再改变时,并不能说明化学反应已达到平衡状态的是( )
A. 混合气体的密度
B. 混合气体的压强
C. 混合气体的总物质的量
D. 混合气体的平均相对分子质量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知 3.6 g 碳在 6.4 g 的氧气中燃烧,至反应物耗尽,并放出 X kJ 热量。已知单质 C(s)的燃烧热数值为 Y kJ·mol-1,则 1 mol C(s)与 O2(g)反应生成 CO(g)的反应热 ΔH 为( )
A. -Y kJ/mol B. -(10X-Y) kJ/mol C. -(5X-0.5Y) kJ/mol D. +(10X-Y) kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某一化工厂以废铁屑为原料制备FeCl3溶液,用作印刷电路铜板腐蚀剂,并对溶液B进行电解处理的实验流程如图:

(1)试剂a应选用________(填写名称);
(2)步骤Ⅰ用到的主要玻璃仪器有漏斗、________(填写仪器名称);
(3)写出步骤Ⅱ中主要反应的化学方程式____________________;
(4)实验室制取气体E的离子方程式是________________________,欲对气体E进行干燥和吸收,需选用下列装置中的________(填写序号);

(5)如何用化学方法检验气体E?______________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com