
| A、溶液 | B、悬浊液 |
| C、胶体 | D、乳浊液 |
 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案科目:高中化学 来源: 题型:
| 实验步骤 | 实验现象及结论 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、摩尔既是表示微粒,又是表示质量的单位 |
| B、1mol氧的质量等于16g |
| C、氢氧化钠的摩尔质量是40g |
| D、氩气的摩尔质量(以g/molWei单位)在数值上等于它的相对原子质量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、次氯酸钙溶液中通入过量CO2:Ca2++2ClO-+H2O+CO2═CaCO3↓+2HClO |
| B、用碳酸钠溶液吸收少量的二氧化硫:2CO32-+SO2+H2O=2HCO3-+SO32- |
| C、用食醋除去水垢中的CaCO3:CaCO3+2H+=Ca2++H2O+CO2↑ |
| D、NH4HCO3溶液与过量的NaOH溶液反应:NH4++OH-=NH3↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
 【物质结构域性质】
【物质结构域性质】查看答案和解析>>
科目:高中化学 来源: 题型:
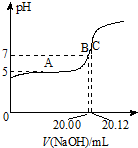 CH3COOH为常见的弱酸,在工业生产和生活中有广泛的应用.
CH3COOH为常见的弱酸,在工业生产和生活中有广泛的应用.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com