
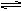 2C(g),当反应达化学平均时,测得有50%的B转化为C,则反应前与平衡时容器内的分子数之比是( )
2C(g),当反应达化学平均时,测得有50%的B转化为C,则反应前与平衡时容器内的分子数之比是( )| A.5∶6 | B.5∶4 | C.5∶3 | D.5∶2 |
科目:高中化学 来源:不详 题型:单选题
| A.加入催化剂有利于氨氧化反应 |
| B.使氢硫酸中加碱有利于S2-离子增多 |
| C.500℃左右比室温更有利于合成氨反应 |
| D.高压条件有利于合成氨 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.V正增大,V逆减小,SO3的百分含量增加 |
| B.V正增大,V逆不变,SO3的百分含量不变 |
| C.V正增大,V逆增大,SO3的百分含量无法判断 |
| D.V正增大,V逆减小,SO3的百分含量保持不变 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
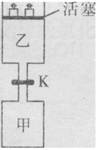
 .1min时反应达平衡状态,有3/4的SO2转化为SO3. 在800℃时,向乙中充入2molSO3.起始时,甲、乙的体积均为1L。下列说法正确的是( )
.1min时反应达平衡状态,有3/4的SO2转化为SO3. 在800℃时,向乙中充入2molSO3.起始时,甲、乙的体积均为1L。下列说法正确的是( )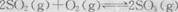 的平衡常数为24
的平衡常数为24查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
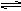 2NH3(g),N2、H2起始分别为10mol、30mol,达平衡时H2的转化率为25%,若从NH3开始反应,在相同条件下,欲使平衡时各成分的体积分数与前者相同,则起始时NH3的物质的量及NH3的转化率为( )
2NH3(g),N2、H2起始分别为10mol、30mol,达平衡时H2的转化率为25%,若从NH3开始反应,在相同条件下,欲使平衡时各成分的体积分数与前者相同,则起始时NH3的物质的量及NH3的转化率为( ) | A.15mol;25% | B.20mol;50% | C.20mol;75% | D.40mol;80% |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 C+D,在t1时增大压强,正、逆反应速率变化图象如图所示,下列有关A、B、C、D的状态叙述正确的是( )
C+D,在t1时增大压强,正、逆反应速率变化图象如图所示,下列有关A、B、C、D的状态叙述正确的是( )
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.不断将氨分离出来 | B.使用催化剂 |
| C.采用500℃左右的高温 | D.采用2×107~5×107Pa的压强 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
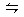 N2O4;ΔH<0。把烧瓶置于100℃的水中,则下列几项性质①颜色;②平均相对分子质量;③质量;④压强;⑤密度。不会改变的是 ( )
N2O4;ΔH<0。把烧瓶置于100℃的水中,则下列几项性质①颜色;②平均相对分子质量;③质量;④压强;⑤密度。不会改变的是 ( )| A.①和③ | B.②和④ | C.④和⑤ | D.③和⑤ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 9 |
| 4 |
| 起始量 | 甲 | 乙 | 丙 |
| H2(mol) | 1 | 2 | 2 |
| CO2(mol) | 1 | 1 | 2 |
| A.反应开始时,甲中的反应速率最慢,丙中的反应速率最快 |
| B.平衡时,甲和丙中CO2的转化率相等,均是60% |
| C.平衡时,乙中H2的转化率大于60% |
| D.平衡时,丙中c(H2)是0.08mol?L-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com