
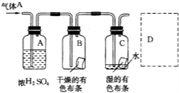
 某生应用如图所示的方法研究物质的性质,其中气体A的主要成分是氯气,杂质是空气和水蒸气.回答下列问题:
某生应用如图所示的方法研究物质的性质,其中气体A的主要成分是氯气,杂质是空气和水蒸气.回答下列问题: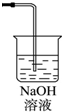 ;
; .
.


 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:
| A、在3mL甲酸浓溶液中加入2滴新制氢氧化铜,加热来检验醛基 |
| B、用加入过量氢氧化钠溶液,振荡、分液的方法除去苯中混有的苯酚杂质 |
| C、将铁屑、溴水、苯混合以制取溴苯 |
| D、除去乙烷中少量的乙烯的方法是:光照条件下通入Cl2,气、液分离 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、淀粉溶液、豆浆、雾和饱和食盐水均可发生丁达尔现象 |
| B、氮化硅(Si3N4)、氧化铝(Al2O3)、碳化硅(SiC)和二氧化锆(ZrO2)都可用作制高温结构陶瓷的材料 |
| C、绿色化学的核心是利用化学原理治理环境污染 |
| D、光化学烟雾、臭氧空洞、温室效应、酸雨(硝酸型)的形成都与氮氧化物有关 |
查看答案和解析>>
科目:高中化学 来源: 题型:
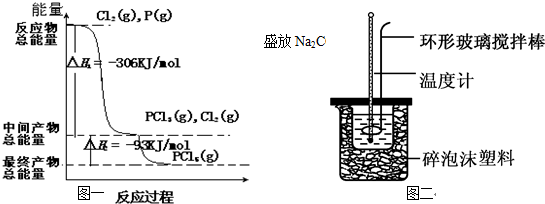
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、m=1,n=5 |
| B、m=3,n=4 |
| C、m=5,n=1 |
| D、m=4,n=5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加入BaCl2溶液,生成白色沉淀,加稀硝酸酸沉淀不消失,则原溶液中一定有SO42- |
| B、加入NaOH溶液并加热,产生使湿润蓝色石蕊试纸变红的气体,则原溶液一定有NH4+ |
| C、通入Cl2后,溶液变为黄色,加入淀粉后溶液变蓝,则原溶液中一定有I- |
| D、加入碳酸钠溶液有白色沉淀生成,再加盐酸,沉淀消失,则原溶液中一定有Ba2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、观察K2SO4的焰色应透过蓝色的钴玻璃 |
| B、Na与NaCl在灼烧时火焰颜色相同 |
| C、可以用焰色反应来区别NaCl和KCl |
| D、焰色反应是元素的性质,属于化学变化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com