
| A. | CO2 | B. | H2 | C. | H2O | D. | O2 |
分析 标准状况下,气体的物质的量n=$\frac{V}{{V}_{m}}$,非气体不能用该公式计算,物质的量越大,所含分子数越多,据此分析.
解答 解:标准状况下,CO2、H2、O2均为气体,其体积相同物质的量相同,设均为1L,则n=$\frac{V}{{V}_{m}}$=$\frac{1}{22.4}$mol,H2O为液体,1L水大约1000g,其物质的量为$\frac{1000g}{18g/mol}$,所以标准状况下,同体积时水的物质的量最大,分子数最多,故C正确.
故选C.
点评 本题考查物质的量有关计算,侧重微粒数目的计算,比较基础,有利于基础知识的巩固,注意把握n=$\frac{V}{{V}_{m}}$的适用范围.


科目:高中化学 来源: 题型:解答题
| HA | H2B | HC | ||
| Ka | Ka1 | Ka2 | Ka3 | Ka4 |
| 数值 | ||||
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验目的 | 实验方法 | |
| A. | 从食盐水中获得食盐 | 过滤 |
| B. | 将海水淡化为可饮用水 | 蒸发 |
| C. | 分离水和碘的四氯化碳溶液 | 分液 |
| D. | 分离碳酸钠溶液和乙酸乙酯 | 萃取 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ag+ H+ NO3- Cl- | B. | Ca2+ NO3- HCO3- Cl- | ||
| C. | K+ H+ Cl- SO42- | D. | Ca2+ Cl-SO42- CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 高锰酸钾在常用危险化学品分类中属于易燃固体 | |
| B. | 实验中不慎打破温度计,可用吹风机加快水银的蒸发 | |
| C. | 做蒸发结晶实验时,用坩埚钳夹持热蒸发皿直接放于实验台面上 | |
| D. | 做分液操作时,待液体分层将下层液体从下口放出后,上层液体从上口倒出 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
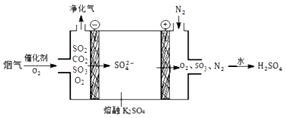 煤炭燃烧中会产生大量烟气容易透成污染,用下图所示的电解池在较高温度下反应,可以净化烟气,月下列列断不正确的是( )
煤炭燃烧中会产生大量烟气容易透成污染,用下图所示的电解池在较高温度下反应,可以净化烟气,月下列列断不正确的是( )| A. | 据图可知,阳极反应式为SO42--2e-=SO2↑+O2↑ | |
| B. | SO2在阴极与O2反应生成硫酸根,则方程式为SO2+O2+2e-=SO42- | |
| C. | 阳极失去2mol电子时,理论上可以得到标准状况下11.2L氧气 | |
| D. | CO2不参与电极反应,净化器中CO2浓度升高 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,2.24 LSO2中所含氧原子数为0.2NA | |
| B. | 将1 mol Cl2通入水中,HC1O、Cl-、ClO-粒子数之和为2NA | |
| C. | 1 mol NO2与足量H2O反应,转移的电子数为NA | |
| D. | 0.1 mol熔融的NaHSO4中阳离子数目为0.lNA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com