

���� ��Ԫ�������ڱ���λ�ã���֪��ΪH����ΪNa����ΪC����ΪN����ΪO����ΪCl��
��1��̼Ԫ�ع����л���γɻ�����������ࣻͬ�����������ԭ�Ӱ뾶��С��ͬ�������϶���ԭ�Ӱ뾶����
��2��Ԫ�طǽ�����Խǿ����Ӧ�⻯��Խ�ȶ���
��3��Ԫ�آڵ��������Ӧ��ˮ����ΪNaOH��������������Ӧ��Cl2+2NaOH=NaCl+NaClO+H2O�����ݷ���ʽ����μӷ�Ӧ�������ʵ�������Ӧ������������������ԭ�����ã���ռ$\frac{1}{2}$�����ClԪ�ػ��ϼ۱仯����ת�Ƶ������ʵ�����
��4��Ԫ�آܺ�Ԫ�آ��γɵ��������ΪNH3��Ԫ�آܵ�����������Ӧ��ˮ����Ϊ���ᣬ���߷�Ӧ��������泥�
��� �⣺��Ԫ�������ڱ���λ�ã���֪��ΪH����ΪNa����ΪC����ΪN����ΪO����ΪCl��
��1��̼Ԫ�ع����л���γɻ�����������ࣻͬ�����������ԭ�Ӱ뾶��С��ͬ�������϶���ԭ�Ӱ뾶��������Ԫ����Naԭ�Ӱ뾶��ʴ�Ϊ���ۣ��ڣ�
��2���ǽ�����O��N��Ԫ�طǽ�����Խǿ����Ӧ�⻯��Խ�ȶ������⻯���ȶ��ԣ�H2O��NH3���ʴ�Ϊ��H2O��NH3��
��3��Ԫ�آڵ��������Ӧ��ˮ����ΪNaOH���������Ӽ������ۼ�������������Ӧ��Cl2+2NaOH=NaCl+NaClO+H2O��NaOH���ʵ���Ϊ$\frac{60g}{40g/mol}$=1.5mol���ʲμӷ�Ӧ�������ʵ���Ϊ$\frac{1.5mol}{2}$=0.75mol����Ӧ������������������ԭ�����ã���ռ$\frac{1}{2}$��ת�Ƶ������ʵ���Ϊ0.75mol��$\frac{1}{2}$��2=0.75mol��
�ʴ�Ϊ��NaOH�����Ӽ������ۼ���0.75��
��4��Ԫ�آܺ�Ԫ�آ��γɵ��������ΪNH3��Ԫ�آܵ�����������Ӧ��ˮ����Ϊ���ᣬ���߷�Ӧ����NH4NO3���ʴ�Ϊ��NH4NO3��
���� ���⿼��Ԫ�����ڱ���Ԫ��������Ӧ�ã�ּ�ڿ���ѧ���Ի���֪ʶ�Ĺ��̣�ע���Ԫ�����ڱ���������գ�


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
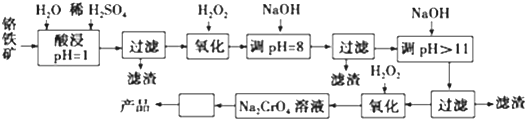
| ������ | Fe3+ | Fe2+ | Mg2+ | Al3+ | Cr3+ |
| ��ʼ����ʱ��pH | 2.7 | 7.6 | 9.0 | -- | -- |
| ������ȫʱ��pH | 3.7 | 9.6 | 11.0 | 8 | 9����9�ܽ⣩ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
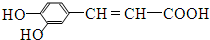 �������йؿ������˵���У�����ȷ���ǣ�������
�������йؿ������˵���У�����ȷ���ǣ�������| A�� | ����������е�����ԭ�Ӳ����ܹ�ƽ�� | |
| B�� | ��������Է�����ԭ���������Ӿۡ���ɫ�ȷ�Ӧ | |
| C�� | 1mol���������4 mol Br2������Ӧ | |
| D�� | 1mol��������NaOH��Һ��Ӧ�������1mol��NaOH |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
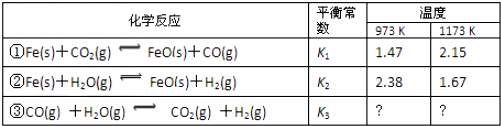
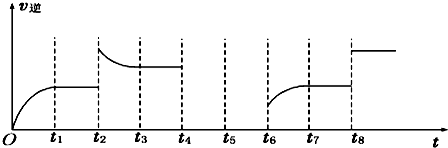
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������̼��ʯ��ˮ��Ӧ��CO2+2OH-�TCO32-+H2O | |
| B�� | ��ˮ��ͨ��������SO2��Br2+SO2+2H2O�T2Br-+SO42-+4H+ | |
| C�� | Cu����ϡ���Cu++2H++NO3-�TCu2++NO2��+H2O | |
| D�� | Na2O2����ˮ����O2��Na2O2+H2O�T2Na++2OH-+O2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������ʱ�����������������ĵ���������ڵ��Ĺ̶� | |
| B�� | ʵ�������Ȼ����Һ������������Һ�����ȡ���� | |
| C�� | ��λ�ѧ���ʶ����ȶ� | |
| D�� | O2��NO��NO2������Ũ��������ͨ��������ܹ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
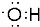 ����CH3��3COH������2-��-2-������ϵͳ��������
����CH3��3COH������2-��-2-������ϵͳ��������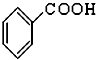 ��CH3CHO ��
��CH3CHO ��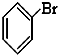
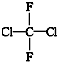 ��
�� 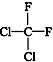 ��
��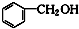 ��
��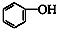 ��CH3CH2NO2��
��CH3CH2NO2��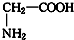
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | ��ѧ��Ӧ | ����ת����ʽ |
| A | CH4+2O2 $\frac{\underline{\;��ȼ\;}}{\;}$CO2+2H2O | ��ѧ��ת�������� |
| B | Pb+PbO2+2H2SO4 $?_{�ŵ�}^{���}$2PbSO4+2H2O | ʹ��ʱ�ŵ磬����ת���ɻ�ѧ�� |
| C | mH2O+nCO2 $��_{Ҷ����}^{��}$Cn��H2O��m+O2 | ����ת���ɻ�ѧ�� |
| D | CaCO3$\frac{\underline{\;����\;}}{\;}$CaO+CO2�� | ����ת���ɻ�ѧ�� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com