
| A. | HOCH2CH2CHO | |
| B. | 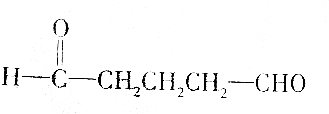 | |
| C. | 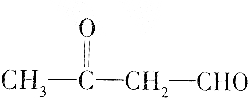 | |
| D. | 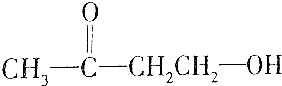 |
分析 有机物甲能发生银镜反应,含有-CHO,为醛或甲酸形成的酯,甲催化加氢还原成有机物乙,则甲中含有不饱和键,1mol乙跟足量的金属钠反应放出标准状况下H222.4L,氢气的物质的量为1mol,说明乙中含有2个羟基或2个羧基或1个羟基、1个羧基,以此来解答.
解答 解:有机物甲能发生银镜反应,含有-CHO,为醛或甲酸形成的酯,甲催化加氢还原成有机物乙,则甲中含有不饱和键,1mol乙跟足量的金属钠反应放出标准状况下H222.4L,氢气的物质的量为1mol,说明乙中含有2个羟基或2个羧基或1个羟基、1个羧基,
A、B、C中物质均含-CHO,均可发生银镜反应,且与氢气发生加成反应后的乙中均含2个-OH,符合题意;
只有选项D不含-CHO,不能发生银镜反应,则甲不可能为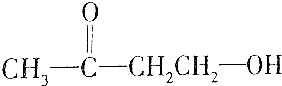 ,
,
故选D.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重分析与应用能力的考查,题目难度不大.


 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol D2O所含质子数为12 NA | |
| B. | 1 mol C16H34中的极性键数为34 NA | |
| C. | 10 g 氖气所含原子数为NA | |
| D. | 22.4 L正戊烷含氢原子数为12 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 新制氯水中加入固体NaOH:c(Na+)=c(Cl-)+c(ClO-)+c(OH-) | |
| B. | pH=8.3的NaHCO3溶液:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) | |
| C. | pH=11的氨水与pH=3的盐酸等体积混合:c(Cl-)=c(NH4+)>c(OH-)=c(H+) | |
| D. | 0.4mol•L-1CH3COOH溶液与0.2mol•L-1NaOH溶液等体积混合:2c(H+)-2c(OH-)=c(CH3COO-)-c(CH3COOH) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
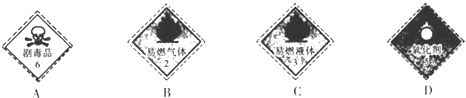
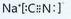 .
.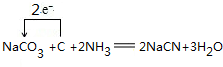 .
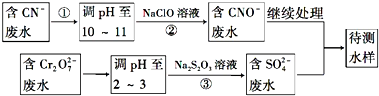
.
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | △H1<0,△H2>0 | B. | 0>△H3>△H4 | ||
| C. | 2△H5+△H1>0 | D. | △H1=△H2+△H3-2△H5 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某温度时,在2L容器中X.、Y、Z三种物质的物质的量随时间变化曲线
某温度时,在2L容器中X.、Y、Z三种物质的物质的量随时间变化曲线查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com