
【题目】李兰娟院士团队公布最新研究成果,阿比朵尔是抗击新型冠状病毒的潜在用药。其合成路线如图:
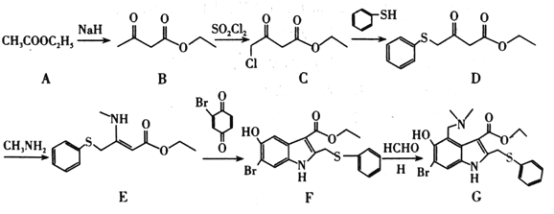
(1)C中含氧官能团的名称为___,G的分子式为___。
(2)A→B的反应类型为___,两分子A生成B和另一种产物,该产物的结构简式为___。
(3)由D生成E的化学方程式为___。
(4)H的结构简式为___。
(5)写出同时符合下列条件的B的所有同分异构体的结构简式:___(不考虑立体异构)。
①能与饱和碳酸氢钠溶液反应产生使澄清石灰水变浑浊的气体
②六元环状结构
(6)结合上述合成路线,设计出以乙醇和![]() 为原料(其他无机试剂任选),合成
为原料(其他无机试剂任选),合成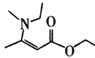 的路线(不超过4步):___。
的路线(不超过4步):___。
【答案】羰基、酯基 C21H23O3N2SBr 取代反应 CH3CH2OH 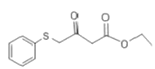 +CH3NH2→
+CH3NH2→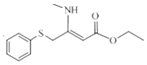 +H2O NH(CH3)2或
+H2O NH(CH3)2或![]()
 、
、 、
、 CH3CH2OH
CH3CH2OH![]() CH3COOH
CH3COOH![]() CH2COOCH2CH3
CH2COOCH2CH3![]()
![]()
![]()
【解析】
CH3COOC2H5在NaH作用下生成B(![]() ),B与SO2Cl2发生取代反应生成C(
),B与SO2Cl2发生取代反应生成C(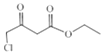 ),C与
),C与![]() 发生取代反应生成D(
发生取代反应生成D(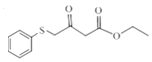 ),D与氨基甲烷(CH3NH2)反应生成E(
),D与氨基甲烷(CH3NH2)反应生成E( ),E与
),E与![]() 反应生成F(
反应生成F(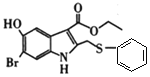 ),F与HCHO及H反应生成产品G(
),F与HCHO及H反应生成产品G( ),则H为NH(CH3)2(或
),则H为NH(CH3)2(或![]() ),以此分析解答。
),以此分析解答。
(1)C为 ,含氧官能团有羰基、酯基,由G的结构简式(
,含氧官能团有羰基、酯基,由G的结构简式( )可知G的分子式为C21H23O3N2SBr,故答案为:羰基、酯基;C21H23O3N2SBr;
)可知G的分子式为C21H23O3N2SBr,故答案为:羰基、酯基;C21H23O3N2SBr;
(2)A→B为CH3COOC2H5在NaH作用下生成![]() ,为两分子A生成B和另一种产物,则A→B为取代反应,另一种产物为CH3CH2OH,故答案为:取代反应;CH3CH2OH;
,为两分子A生成B和另一种产物,则A→B为取代反应,另一种产物为CH3CH2OH,故答案为:取代反应;CH3CH2OH;
(3)D与氨基甲烷反应生成E 和水,D生成E的反应方程式为:
和水,D生成E的反应方程式为: +CH3NH2→
+CH3NH2→ +H2O,故答案为:
+H2O,故答案为: +CH3NH2→
+CH3NH2→ +H2O;
+H2O;
(4)F与HCHO和H反应生成G(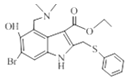 ),根据G和F的结构的区别可知,H为:NH(CH3)2或
),根据G和F的结构的区别可知,H为:NH(CH3)2或![]() ,故答案为:NH(CH3)2或
,故答案为:NH(CH3)2或![]() ;
;
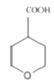
(5)B为![]() 。①与碳酸氢钠反应产生使澄清石灰水变浑浊的气体,说明结构中有羧基(-COOH),②六元环状结构,B分子中总共有6个碳,羧基中须含有一个碳,则六元环中有一个氧原子,满足条件的B的同分异构体有
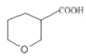
。①与碳酸氢钠反应产生使澄清石灰水变浑浊的气体,说明结构中有羧基(-COOH),②六元环状结构,B分子中总共有6个碳,羧基中须含有一个碳,则六元环中有一个氧原子,满足条件的B的同分异构体有![]() 、
、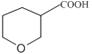 、
、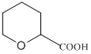 ,故答案为:
,故答案为:![]() 、
、 、
、 ;
;
(6)由乙醇和![]() 合成
合成 ,根据题意,需要先合成乙酸乙酯,原料中有乙醇,乙醇氧化可以合成乙酸,则合成流程为CH3CH2OH
,根据题意,需要先合成乙酸乙酯,原料中有乙醇,乙醇氧化可以合成乙酸,则合成流程为CH3CH2OH![]() CH3COOH
CH3COOH![]() CH2COOCH2CH3
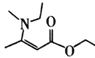
CH2COOCH2CH3![]()
![]()
![]()
 ,故答案为:CH3CH2OH
,故答案为:CH3CH2OH![]() CH3COOH
CH3COOH![]() CH2COOCH2CH3
CH2COOCH2CH3![]()
![]()
![]()
 。
。


科目:高中化学 来源: 题型:
【题目】某固体混合物可能含有![]() 、
、![]() 、
、![]() 、
、![]() 和
和![]() 中的一种或几种,将该混合物进行如下实验:
中的一种或几种,将该混合物进行如下实验:
①将少许混合物放入水中得到无色溶液和白色沉淀,过滤;
②取溶液进行焰色反应,火焰呈黄色;
③取白色沉淀加入稀盐酸,沉淀完全溶解并放出气体
由上述现象推断:
(1)该混合物中一定含有________,一定不含有________,可能含有________。
(2)若要检验可能含有的物质是否存在,可以采用的实验操作为_____(填写字母)。
A.取步骤①中滤液,加入![]() 溶液
溶液
B.取步骤①中滤液,加入NaOH溶液
C.取步骤①中滤液,加入足量![]() 溶液,静置后在上层清液中加入硝酸酸化
溶液,静置后在上层清液中加入硝酸酸化![]() 溶液
溶液
D.取步骤①中滤液,加入足量![]() 溶液,静置后上层清液中加入硝酸酸化
溶液,静置后上层清液中加入硝酸酸化![]() 溶液
溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】0.096 kg碳完全燃烧生成CO2气体可放出3147.9 kJ的热量,则下列热化学方程式正确的是( )
A. C(s)+O2(g)===CO2(g) ΔH=-393.49 kJ/mol
B. C(s)+O2(g)===CO2(g) ΔH=+393.49 kJ/mol
C. C+O2===CO2 ΔH=-393.49 kJ/mol
D. C(s)+![]() O2(g)===CO(g) ΔH=-393.49 kJ/mol
O2(g)===CO(g) ΔH=-393.49 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素Q、R、T、W在元素周期表中的位置如图,其中T原子的M层电子数比K层多2个,下列叙述不正确的是( )
![]()
A. 氢化物的稳定性:R<Q<T
B. T的单质是一种良好的半导体材料
C. Q、R的简单氢化物分子所含质子数、电子数与氖原子相同
D. T、W的最高价氧化物的水化物的酸性W强于T
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制取氯气,将多余的氯气用100 mL 1.7mol/L的NaOH溶液完全吸收。对吸收后的溶液进行分析化验,测知c(OH-)=0.1mol/L (不考虑反应前后溶液的体积变化) 。ClO-和ClO3-的物质的量浓度之比为5∶1。请回答:
(1)吸收氯气消耗的NaOH的物质的量为_______________mol。
(2)被氧化的氯气的物质的量为_______________mol,被还原的氯气的物质的量为 _______________mol。
(3)若采用二氧化锰和浓盐酸共热的方法制氯气,制备尾气中的氯气所消耗的二氧化锰的质量为_______________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①H2(g)+![]() O2(g)=H2O(g) ΔH1=akJ·mol1
O2(g)=H2O(g) ΔH1=akJ·mol1
②2H2(g)+O2(g)=2H2O(g) ΔH2=bkJ·mol1
③H2(g)+![]() O2(g)=H2O(l) ΔH3=ckJ·mol1
O2(g)=H2O(l) ΔH3=ckJ·mol1
④2H2(g)+O2(g)=2H2O(l) ΔH4=d kJ·mol1
下列关系式中正确的是
A.a<c<0B.b>d>0C.2a=b<0D.2c=d>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组利用如图装置进行铁与水蒸气反应的实验,并检验产物的性质,请回答下列问题:

(1)A装置的作用是____________,烧瓶底部放碎瓷片的作用是_________________________。
(2)装置B中发生反应的化学方程式是____________________________________,该反应中氧化剂是__________,氧化产物是__________________。
(3)D的作用是__________________________________。
(4)E中的实验现象是____________________________。
(5)A、B两个装置中应先点燃________________处的酒精(喷)灯,点燃E处酒精灯之前应进行的操作是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组模拟“侯氏制碱法”,以NaCl、NH3、CO2和水等为原料以及图1所示装置制取NaHCO3,反应的化学方程式为NH3+CO2+H2O+NaCl===NaHCO3↓+NH4Cl,然后再将NaHCO3制成Na2CO3。

(1)装置乙的作用是______________________________________。为防止污染空气,尾气中含有的______________需要进行吸收处理。
(2)由装置丙中产生的NaHCO3制取Na2CO3时,需要进行的实验操作有________________、洗涤、灼烧。
(3)若在(2)中灼烧的时间较短,NaHCO3将分解不完全,该小组对一份加热了t1min的NaHCO3样品的组成进行了研究。取加热了t1min的NaHCO3样品29.6 g完全溶于水制成溶液,然后向此溶液中缓慢地滴加稀盐酸,并不断搅拌,随着盐酸的加入,溶液中有关离子的物质的量的变化如图2所示,则曲线c对应的溶液中的离子是______________________(填离子符号);该样品中NaHCO3和Na2CO3的物质的量之比是__________。
(4)若取10.5 g NaHCO3固体,加热了t1min后,剩余固体的质量为7.4 g。如果把此剩余固体全部加入到200 mL 1 mol·L-1的盐酸中,则充分反应后溶液中H+的物质的量浓度为__________(设溶液体积变化忽略不计)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一体积可变的密闭容器中,加入一定量的X,Y,Z,发生反应mX(g)+nY(g) pZ(g) ΔH=QkJ·mol-1。反应达到平衡后,Y的物质的量浓度与温度、容器体积的关系如下表所示。下列说法不正确的是

A.![]() B.体积不变,温度升高,平衡向逆反应方向移动
B.体积不变,温度升高,平衡向逆反应方向移动
C.Q<0D.温度不变,压强增大,Y的质量分数增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com