
【题目】(选修5——有机化学基础)
呋喃(C4H4O)是生产抗流感药物磷酸奥司他韦(又名达菲)的原料之一,以玉米芯为原料制备呋喃及相关衍生物的一种工艺流程如下:
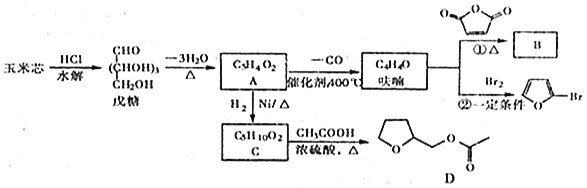
已知:ⅰ)A可以发生银镜反应
ⅱ)![]()
(1)D的分子式为___________________。
(2)呋喃的结构简式为___________;②的反应类型为________________。
(3)A发生银镜反应的化学方程式 ____________________________________________。
(4)C生成D的化学方程式__________________________________________。
(5)反应①在有机合成中具有重要意义,则B的结构简式为__________ 。
(6)C的同分异构体中,含有“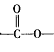 ”结构的共有____________ 种(不含立体导构),其中能发生很镜反应,且核磁共振氢谱中有2组吸收峰的有机物的结构简式为________ 。
”结构的共有____________ 种(不含立体导构),其中能发生很镜反应,且核磁共振氢谱中有2组吸收峰的有机物的结构简式为________ 。
【答案】C7H12O3![]() 取代反应
取代反应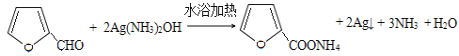
![]() +CH3COOH
+CH3COOH![]()
![]() +H2O
+H2O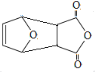 13
13
【解析】
(1)由D的键线式为得其分子式为:C7H12O3,故答案为:C7H12O3;
(2)由反应②可得物质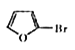 推断呋喃的结构简式为
推断呋喃的结构简式为![]() ,反应②为取代反应,故答案为:
,反应②为取代反应,故答案为:![]() 、取代反应;
、取代反应;
(3)A的结构简式为:![]() ,发生银镜反应的方程式为:
,发生银镜反应的方程式为:![]() ;
;
(4)C生成D的反应类型为酯化反应,方程式为:![]() +CH3COOH
+CH3COOH![]()
![]() +H2O;
+H2O;
(5)由题给信息可知反应①为共轭二烯烃的加成反应,则B的结构简式为: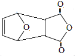 ;
;
(6)分子式符合C5H10O2且分子含有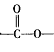 结构的有机化合物可能是羧酸,也有可能是酯类物质,因-C4H9有四种结构,则C4H9-COOH有四种结构,HCOO-C4H9也有四种结构,C3H7-有两种结构,则CH3COO-C3H7与CH3OOC-C3H7分别有两种结构,CH3CH2COO-C2H5只有一种结构,故C的同分异构体中,含有“
结构的有机化合物可能是羧酸,也有可能是酯类物质,因-C4H9有四种结构,则C4H9-COOH有四种结构,HCOO-C4H9也有四种结构,C3H7-有两种结构,则CH3COO-C3H7与CH3OOC-C3H7分别有两种结构,CH3CH2COO-C2H5只有一种结构,故C的同分异构体中,含有“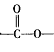 ”结构的共有13种;其中能发生很镜反应,说明属于甲酸酯,核磁共振氢谱中有2组吸收峰说明分子中只有两种不同化学环境下的氢原子,其结构简式为:
”结构的共有13种;其中能发生很镜反应,说明属于甲酸酯,核磁共振氢谱中有2组吸收峰说明分子中只有两种不同化学环境下的氢原子,其结构简式为: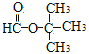 ;故答案为:13、
;故答案为:13、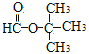 。
。


 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案科目:高中化学 来源: 题型:
【题目】 2004年12月26日,印度洋发生海啸,灾民饮用水被严重污染,急需进行净化处理。下列净化水的单一操作中,净化程度最高的是
A.蒸馏B.吸附沉淀C.过滤D.静置沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组查阅资料得知,漂白粉与硫酸溶液反应可制取氯气,化学方程式为:Ca(ClO)2+ CaCl2+ 2H2SO4 ![]() 2CaSO4 + 2Cl2↑+ 2H2O,他们设计如下实验用于制取氯气并验证其性质。
2CaSO4 + 2Cl2↑+ 2H2O,他们设计如下实验用于制取氯气并验证其性质。

试回答:
(1)该实验中A部分的装置是________(填写装置的序号)。
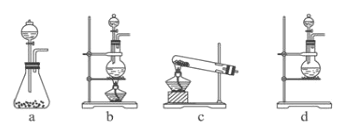
(2)B中的实验现象为___________________________ 。
(3)用离子方程式表示C中亚硫酸钠被氧化的主要原因,_____________________。请你帮助他们设计一个实验,证明洗气瓶C中的亚硫酸钠已被氧化(简述实验步骤)_____________。
(4)请根据题意画出D处的实验装置图,并注明盛放的物质______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溴、碘主要存在于海水中,有“海洋元素”的美称。海水中的碘富集在海藻中,我国海带产量居世界第一,除供食用外,大量用于制碘。提取碘的途径如下所示:
干海带![]() 海带灰
海带灰![]() 水溶液
水溶液![]()
![]()
![]() ―→碘单质
―→碘单质
下列有关叙述正确的是( )
A. 碘元素在海水中也有游离态存在 B. 在提取的过程中用的氧化剂可以是H2O2
C. 操作A是结晶或重结晶 D. B是提纯操作,常用蒸馏或分馏
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钼是一种重要的过渡金属元素,通常用作合金及不锈钢的添加剂,可增强合金的强度、硬度、可焊性等。钼酸钠晶体(Na2MoO4·2H2O)可作为无公害型冷却水系统的金属腐蚀抑制剂,如图15是化工生产中以辉钼矿(主要成分为硫化钼MoS2)为原料来制备金属钼、钼酸钠晶体的主要流程图。
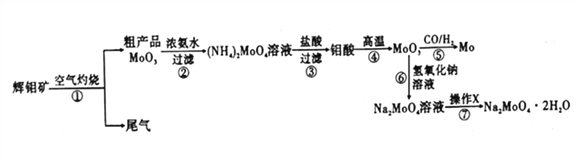
回答下列问题:
(1)已知反应③为复分解反应,则钼酸中钥的化合价为___________。
(2)反应⑥的离子方程式为___________。
(3)辉钼矿灼烧时的化学方程式为____________。
(4)操作X为_________。已知钼酸钠在一定温度范围内的析出物质及相应物质的溶解度如下表所示,则在操作X中应控制温度的最佳范围为_______(填序号)。
温度(℃) | 0 | 4 | 9 | 10 | 15.5 | 32 | 51.5 | 100 | >100 |
析出物质 | Na2MoO4·10H2O | Na2MoO4·2H2O | Na2MoO4 | ||||||
溶解度 | 30.63 | 33.85 | 38.16 | 39.28 | 39.27 | 39.82 | 41.27 | 45.57 | |
A.0℃~10℃ B.10℃~100℃ C.15.5℃~50℃ D.100℃以上
(5)制备钼酸钠晶体还可用通过向精制的辉钼矿中直接加入次氯酸钠溶液氧化的方法,若氧化过程中,还有硫酸钠生成,则氧化剂与还原剂的物质的量之比为_________。
(6)Li、MoS2可充电电池的工作原理为xLi+nMoS2![]() Lix(MoS2)n[Lix(MoS2)n附着在电极上],则电池充电时阳极的电极反应式为___________________。
Lix(MoS2)n[Lix(MoS2)n附着在电极上],则电池充电时阳极的电极反应式为___________________。
(7)可用还原性气体(CO和H2)还原MoO3制钼,业上制备还原性气体CO和H2的反应原理之一为CO2+CH4![]() 2CO+2H2。含甲烷体积分数为90%的7L(标准状况)天然气与足量二氧化碳在高温下反应,甲烷转化率为80%,用产生的CO和H2还原MoO3制钼,理论上能生产钼的质量为_________。
2CO+2H2。含甲烷体积分数为90%的7L(标准状况)天然气与足量二氧化碳在高温下反应,甲烷转化率为80%,用产生的CO和H2还原MoO3制钼,理论上能生产钼的质量为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把下列物质分别加入盛水的锥形瓶,立即塞紧带U形管的塞子。已知U形管内预先装有少量水且液面相平(为便于观察,预先染成红色),加入下列哪些物质后,发生如如图所示变化( )

① NH4NO3晶体 ② 浓H2SO4 ③ NaOH粉末
④ NaCl晶体 ⑤ Na2O2固体 ⑥ 生石灰
A. ①②④⑤ B. ①②③
C. ③④⑤ D. ②③⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C是由周期表中短周期元素组成的三种常见化合物,甲、乙、丙是三种单质,这些单质和化合物之间存在如图所示的关系,完成下列空白:
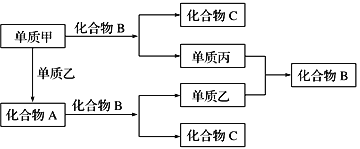
(1)向酚酞试液中加入化合物A的粉末,现象为________。
(2)单质甲与化合物B反应的离子方程式为__________。5.05g单质甲—钾合金溶于200mL水生成0.075mol氢气,确定该合金的化学式为______ 。
(3)向一定体积某浓度的化合物C的溶液中通人CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也不同。若向M中逐滴加入0.1mol/L盐酸,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)的关系有下列图示两种情况。
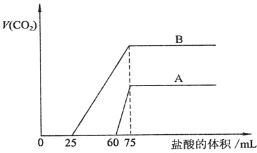
①由A确定滴加前60mL的盐酸时,发生反应的离子方程式为_____________________
②B对应的溶液M低温蒸干后得到固体a克,将a克固体充分加热至恒重后,固体质量减少 _____ 克。
③由A、B可知,两次实验通入的CO2的体积比为___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,将3 mol A和1 mol B两种气体混合于固定容积为2 L的密闭容器中,发生如下反应:3A(g)+B(g)![]() xC(g)+2D(g)。2 min末该反应达到平衡,测得生成0.8 mol D, 0.4 mol C。下列判断不正确的是
xC(g)+2D(g)。2 min末该反应达到平衡,测得生成0.8 mol D, 0.4 mol C。下列判断不正确的是
A. x =1
B. 2 min时,A的浓度为0.9mol·L-1
C. 2 min内A的反应速率为0.3 mol·L-1·min-1
D. B的转化率为60%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com