
【题目】乐山某高中化学兴趣小组同学用西红柿(或洋葱)作为供水剂,设计了如图装置验证铁与水蒸气的反应,并对产物进行检验。回答下列问题:
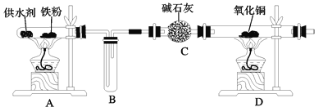
(1)A中铁与水蒸气反应的化学方程式是__。
(2)C中碱石灰的作用是__。
(3)D处实验现象为__。
(4)上述实验结束后,取出A中铁粉反应后的少量固体继续进行如下实验:
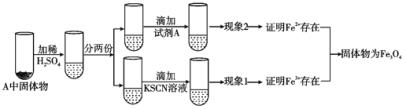
(Ⅰ)固体A中Fe3O4与稀硫酸反应的离子方程式为__。
(Ⅱ)试剂A是__(选填字母)。
a.NaOH溶液 b.酸性KMnO4溶液 c.酚酞 d.新制氯水
(Ⅲ)有同学认为;即使得到了现象1和现象2的实验现象,也不能确定所得固体成分为Fe3O4。你认为该同学持此看法的理由是__。
【答案】3Fe+4H2O(g)![]() Fe3O4+4H2 干燥H2 黑色固体变为红色,管壁有水珠出现 Fe3O4+8H+=Fe2++2Fe3++4H2O b 过量的Fe粉与稀盐酸反应也会生成Fe2+
Fe3O4+4H2 干燥H2 黑色固体变为红色,管壁有水珠出现 Fe3O4+8H+=Fe2++2Fe3++4H2O b 过量的Fe粉与稀盐酸反应也会生成Fe2+
【解析】
根据铁与水蒸气反应生成四氧化三铁和氢气的原理、三价铁离子与二价亚铁离子的检验方法进行分析即可。
(1)A中铁与水蒸气反应生成四氧化三铁和氢气,反应的化学方程式为3Fe+4H2O(g)![]() Fe3O4+4H2;
Fe3O4+4H2;
(2)氢气还原氧化铜之前需要干燥,则C中碱石灰的作用是干燥H2;
(3)D处高温条件下氢气还原氧化铜生成铜单质和水,实验现象为黑色固体变为红色,管壁有水珠出现;
(4) (Ⅰ)加入稀硫酸后四氧化三铁与硫酸反应生成硫酸铁、硫酸亚铁和水,发生的离子方程式为Fe3O4+8H+=Fe2++2Fe3++4H2O;
(Ⅱ)根据结论说明加入试剂A为检验Fe2+的存在,Fe2+具有还原性,在有Fe3+存在的条件下进行检验,故试剂A为酸性KMnO4溶液;答案选b;
(Ⅲ)由于过量的Fe粉与稀盐酸反应也会生成Fe2+,所以即使得到了现象1和现象2的实验现象,也不能确定所得固体成分为Fe3O4。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】某溶液中可能含有Na+、NH4+、SO42-、SO32-、Cl-、Fe2+、Fe3+、CO32-中的若干种,且各离子浓度均相同。为确定其组成现进行如下实验:
①向溶液中加入足量硝酸酸化的Ba(NO3)2溶液,产生白色沉淀,过滤
②向①中的滤液加入足量NaOH溶液,有沉淀生成,微热,有气体产生
下列说法正确的是( )
A.无法确定原溶液中是否存在SO32-
B.是否存在![]() 需要通过焰色反应来确定
需要通过焰色反应来确定
C.CO32-肯定不存在,Fe2+、Fe3+至少有一种
D.溶液中存在NH4+、SO42-、Cl-、Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜能与浓硫酸在加热条件下反应,反应方程式为:
_____Cu +____H2SO4(浓) ![]() _____CuSO4 +____SO2↑+_____H2O
_____CuSO4 +____SO2↑+_____H2O
(1)配平上述方程式,并用双线桥法分析电子转移的方向和数目___________(在答题卷上的方程式中表示);
(2)该反应中还原剂为___________,氧化产物为__________;
(3)该反应中浓H2SO4体现____________性;
(4)还原剂与氧化剂的物质的量之比为______,标况下若生成SO2的体积为11.2 L,则反应时转移的电子为_______ mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚合硫酸铁[Fe(OH)SO4]n能用做净水剂(絮凝剂),可由绿矾(FeSO47H2O)和KClO3在水溶液中反应得到。下列说法不正确的是( )
A.KClO3作氧化剂,每生成1mol[Fe(OH)SO4]n消耗![]() molKClO3
molKClO3
B.生成聚合硫酸铁后,水溶液的pH增大
C.聚合硫酸铁可在水溶液中水解生成氢氧化铁胶体而净水
D.在反应中氧化剂和还原剂物质的量之比为1:6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用有机物甲可制备环己二烯(![]() ),其反应路线如图所示:
),其反应路线如图所示:

下列有关判断不正确的是
A.甲的分子式为 C6H12
B.乙与环己二烯互为同系物
C.上述流程发生的反应类型有取代反应、消去反应、加成反应
D.环己二烯与溴水 1:1 反应可得 2 种产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素甲 ~ 辛在周期表中的位置如表所示,下列说法错误的是( )

A.元素甲、丁、戊的单质都是金属
B.元素乙、丙、辛都是非金属元素
C.元素乙、庚、辛都能形成氧化物
D.己的氧化物既可溶于![]() 溶液又可溶于稀硫酸
溶液又可溶于稀硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据部分短周期元素的信息回答问题。
元素 | 元素信息 |
A | 第3周期ⅣA族 |
B | 族序数是周期数的3倍 |
C | 原子序数是11 |
D | D3+与Ne的电子数相同 |
(1)A、B的元素符号分别为__、__,C、D的元素名称分别为__、__。
(2)写出B、C的常见单质在加热时的反应方程式:__。
(3)从原子结构的角度分析,A原子与B原子的__相同,C原子与D原子的__相同。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列描述中正确的是
①CS2为V形的极性分子
②ClO3-的空间构型为平面三角形
③SF6中有6对完全相同的成键电子对
④SiF4和SO32-的中心原子均为sp3杂化
A.①②B.②③C.③④D.①④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】鸟粪石[化学式为Mg(NH4)PO4·6H2O]是一种盛产于秘鲁的优质氮磷肥料;钴(Co)是质子数为27的元素,它的中子数为33的核素可用于癌症的放射性治疗。下列有关说法正确的是
①钴不是主族元素;②![]() Cl2不能长期稳定地存在;③Mg的原子结构示意图为
Cl2不能长期稳定地存在;③Mg的原子结构示意图为 ;④鸟粪石中两种阳离子为Mg2+、NH4+
;④鸟粪石中两种阳离子为Mg2+、NH4+
A.①②③④B.仅①②④C.仅②③④D.仅①③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com