
| T/K | 303 | 313 | 323 |
| NH3生成量/(10-6mol) | 4.8 | 5.9 | 6.0 |


分析 (1)该反应是反应前后气体体积减小的、放热的可逆反应,要提高二氧化氮的转化率,只要改变条件使化学平衡向正反应方向移动即可;
(2)由表中数据可知,升高温度,NH3生成量增大,说明平衡向正反应方向移动,结合反应方程式中各物质的聚集状态解答;
(3)①已知总反应的快慢由慢的一步决定,结合图象变化趋势,图象表达反应的判断,反应快慢可以依据第一步和第二步反应的曲线斜率比较大小;当氨基甲酸铵、尿素物质的量不再变化时,反应达到平衡;
②根据图象中二氧化碳在10 min时测得CO2的物质的量计算出用CO2表示的第一步反应的速率v(CO2);
(4)根据化学方程式的系数进行回答;
(5)①根据盖斯定律,由已知热化学方程式乘以适当的系数进行加减构造目标热化学方程式;
②根据体系中进入的物质和得到的物质获得反应物和生成物,利用氧化还原方程式的配平写出化学方程式;根据溶液中阳离子的移动判断电子的流向.
解答 解:(1)该反应是反应前后气体体积减小的、放热的可逆反应,要使该反应向正反应方向移动,可改变反应物的浓度、体系的压强、温度等.
A、减小N02的浓度,平衡向逆反应方向移动,N02的转化率降低,故A错误;
B.降低温度,平衡向正反应方向移动,N02的转化率提高,故B正确;
C.增加N02的浓度,平衡向正反应方向移动,且体系压强增大,也利于反应向正反应方向移动,故C正确;
D.升高温度,平衡向逆反应方向移动,N02的转化率降低,故D错误;
故答案为:BC;
(2)由表中数据可知,升高温度,NH3生成量增大,说明平衡向正反应方向移动,则正反应应为吸热反应,a>0,由方程式可知反应生成气体的物质的量增多,则△S>0,故答案为:>;>;
(3)①由图象可知在15分钟左右,氨气和二氧化碳反应生成氨基甲酸铵后不再变化发生的是第一步反应,氨基甲酸铵先增大再减小最后达到平衡,发生的是第二部反应,从曲线斜率不难看出第二部反应速率慢,所以已知总反应的快慢由慢的一步决定,则合成尿素总反应的快慢由第二步决定,由图象变化可知当进行到55分钟时,反应达到平衡,
故答案为:2;55;
②反应进行到10 min时测得CO2的物质的量为0.26mol,二氧化碳的浓度变化为:c(CO2)=$\frac{1mol-0.26mol}{0.5L}$=1.48mol/L,则用CO2表示的第一步反应的速率v(CO2)=$\frac{1.48mol/L}{10min}$=0.148 mol/(L•min),
故答案为:0.148 mol/(L•min);
(4)CH3OCH3的体积分数随投料比[n(H2)/n(CO2)]的增大而增大,根据反应知道当体积比是3的时候,甲醚的体积分数最大,如下图所示: ,故答案为:
,故答案为: ;
;
(5)①已知:CH4(g)+2NO2(g)═N2(g)+CO2(g)+2H2O(g)△H1=-867kJ/mol①
2NO2(g)?N2O4(g)△H2=-56.9kJ/mol②
根据盖斯定律,①-②可得CH4(g)+N2O4(g)=N2(g)+CO2(g)+2H2O(g),故△H=-867kJ/mol-(-56.9kJ/mol)=-810.1kJ/mol 即CH4(g)+N2O4(g)═N2(g)+2H2O(g)+CO2(g)△H=-810.1kJ/mol,
故答案为:CH4(g)+N2O4(g)═N2(g)+2H2O(g)+CO2(g)△H=-810.1kJ/mol;
②体系中进入的物质为:CO2和H2O,则反应物为:CO2和H2O,得到的物质为:HCOOH和O2,生成物为:HCOOH和O2,利用氧化还原方程式的配平写出化学方程式为:2CO2+2H2O$\frac{\underline{\;光照\;}}{\;}$2HCOOH+O2;体系中氢离子从a→b,则电流的方向为:b→a,电子的流向为a→b,故答案为:2CO2+2H2O$\frac{\underline{\;光照\;}}{\;}$2HCOOH+O2;a→b.
点评 本题考查化学平衡计算、反应热计算、影响化学平衡因素分析判断,注意利用电子转移守恒计算,掌握基础是解题关键,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 铀元素一定至少还存在一种质量数大于238的同位素,X为中子 | |
| B. | 不能用质量数代替铀的同位素的相对原子质量计算它的近似相对原子质量,X为原子 | |
| C. | 黔U的变化属于化学变化,X为质子 | |
| D. | 铀的几种同位素的化学性质明显不同,X为电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al2(SO4)3═Al23++3SO42- | B. | NaHSO4═Na++HSO4- | ||
| C. | NaHCO3═Na++H++CO32- | D. | Na3PO4═3Na++PO43- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③⑤ | B. | ②④ | C. | ③⑤ | D. | ②③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
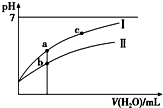 已知:25℃时某些弱酸的电离平衡常数(如表).下面图象表示常温下,稀释CH3COOH、HClO两种酸的稀溶液时,溶液pH随加水量的变化.下列说法正确的是( )
已知:25℃时某些弱酸的电离平衡常数(如表).下面图象表示常温下,稀释CH3COOH、HClO两种酸的稀溶液时,溶液pH随加水量的变化.下列说法正确的是( ) | CH3COOH | HClO | H2CO3 |
| Ka=1.8×10-5 | Ka=3.0×10-8 | Ka1=4.1×10-7 Ka2=5.6×10-11 |
| A. | 相同浓度CH3COONa和NaClO的混合液中,各离子浓度的大小关系是c(Na+)>c(ClO-)>c(CH3COO-)>c(OH-)>c(H+) | |
| B. | 向NaClO溶液中通入少量二氧化碳的离子方程式为:2ClO-+CO2+H2O═2HClO+CO32- | |
| C. | 图象中a、c两点处的溶液中$\frac{c({R}^{-})}{c(HR)•c(O{H}^{-})}$相等(HR代表CH3COOH或HClO) | |
| D. | 图象中a点酸的总浓度大于b点酸的总浓度 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
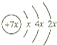 ,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.
,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有① | B. | ①③④ | C. | ②④⑥ | D. | 只有⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
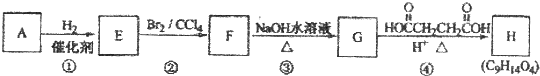
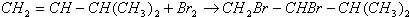 ;
;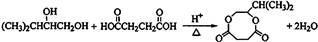 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com