


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
A、KOH(aq)+
| ||||
| B、2KOH(s)+H2SO4(aq)=K2SO4(aq)+2H2O (l);△H=-114.6kJ/mol | ||||
| C、2KOH(aq)+H2SO4=K2SO4(aq)+H2O (l);△H=+114.6kJ/mol | ||||
D、KOH (aq)+
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、明矾水解时产生具有吸附性的胶体粒子,可以用于饮用水的杀菌消毒 |
| B、SiO2制成的玻璃纤维,由于导电能力强而被用于制造通讯光缆 |
| C、鼓励汽车、家电“以旧换新”,可减少环境污染,发展循环经济,促进节能减排 |
| D、焰火“脚印”、“笑脸”,使北京奥运会开幕式更加辉煌、浪漫,这与高中化学中“焰色反应”的知识相关,焰色反应是化学变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
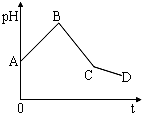 将等物质的量浓度的CuSO4溶液和NaCl溶液等体积混合后,用石墨电极进行电解,电解过程中,溶液pH随时间t变化的曲线如图,则下列说法正确的是( )
将等物质的量浓度的CuSO4溶液和NaCl溶液等体积混合后,用石墨电极进行电解,电解过程中,溶液pH随时间t变化的曲线如图,则下列说法正确的是( )| A、整个过程中阳极先产生Cl2,后产生O2 |
| B、阳极极产物一定是Cl2,阴极产物一定是Cu |
| C、BC段表示在阴极上是H+放电产生了H2 |
| D、CD段表示阳极上OH一放电破坏了水的电离平衡,产生了H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
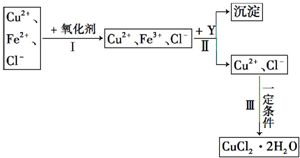 CuCl2溶液中含有少量杂质FeCl2,为制备纯净的CuCl2?2H2O晶体,拟定实验步骤如图所示:请回答下列问题:
CuCl2溶液中含有少量杂质FeCl2,为制备纯净的CuCl2?2H2O晶体,拟定实验步骤如图所示:请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在密闭容器中,N2+3H2?2NH3以达到平衡时,c(NH3) 与c(N2)之比 |
| B、常温下,pH=12的NH3?H2O和Ba(OH)2溶液的物质的量浓度之比 |
| C、常温下,物质的量浓度相同的NH3?H2O和Ba(OH)2溶液的c(OH-)之比 |
| D、常温下,pH=7的(NH4)2SO4和NH3?H2O混合溶液中c(NH4+)与c(SO42-)之比 |
查看答案和解析>>
科目:高中化学 来源: 题型:
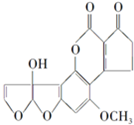 黄曲霉毒素M1是一种具有强致癌性的有机物,其分子结构如图所示.下列有关黄曲霉毒素M1的说法正确的是( )
黄曲霉毒素M1是一种具有强致癌性的有机物,其分子结构如图所示.下列有关黄曲霉毒素M1的说法正确的是( )| A、黄曲霉毒素M1的分子式为C17H14O7 |
| B、黄曲霉毒素M1含有羟基,此羟基能被催化氧化为醛基 |
| C、1 mol黄曲霉毒素M1与NaOH溶液发生反应最多能消耗2 mol NaOH |
| D、1 mol黄曲霉毒素M1最多能与7 mol H2发生加成反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com