
| A、Cu |
| B、CO2 |
| C、冰醋酸 |
| D、氨水 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、NaCl(Na2CO3):溶解,滴入足量盐酸,蒸发结晶 |
| B、Na2SO4(NH4Cl):加热、升华 |
| C、CO2(CO):通过灼热CuO粉末 |
| D、H2(NH3):通过盛浓H2SO4的洗气瓶 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、先与HBr加成后再与HCl加成 |
| B、先与H2完全加成后再与Cl2、Br2取代 |
| C、先与HCl加成后再与Br2加成 |
| D、先与Cl2加成后再与HBr加成 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、10min内NO浓度变化表示的速率v(NO)=0.01 mol?L-1?min-1 |
| B、若保持其他条件不变,在恒压下进行该反应,则平衡时NO2的转化率大于50% |
| C、若升高温度,平衡逆向移动,则该反应的△H>0 |
| D、若起始时向容器中充入NO2(g)0.2mol、NO(g)0.1mol和Cl2(g)0.1mol(固体物质足量),则反应将向逆反应方向进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钢铁制品腐蚀时正极反应:O2+2H2O+4e-=4OH- |
| B、在酸性较强的溶液中,金属主要发生析氢腐蚀 |
| C、为减缓金属腐蚀,可将要保护的金属物件与外电源的正极相连接 |
| D、在海轮外壳上附着一些锌块,则可以减缓海轮外壳的腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、实验室配制FeCl3溶液时用盐酸溶解FeCl3固体 |
| B、向沸水中滴加饱和FeCl3溶液加热至红褐色制得Fe(OH)3胶体 |
| C、短期保存FeCl2溶液时向其中加入少量铁粉 |
| D、保存Na2CO3溶液的试剂瓶用橡胶塞而不能用玻璃塞 |
查看答案和解析>>
科目:高中化学 来源: 题型:
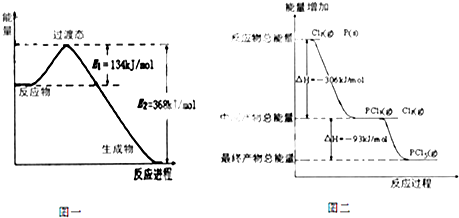
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com