
| A. | 该混合溶液中有:c(Na+)+c(H+)=c(HC2O4-)+c(OH-)+2 c(C2O42-) | |
| B. | 该混合溶液中有:c( Na+)=2[c(HC2O4-)+c(H2C2O4)+c(C2O42-)] | |
| C. | 该混合溶液中有:c(OH-)-c(H+)=c(HC2O4-)+2 c(H2C2O4) | |
| D. | 该混合溶液中有:c(Na+)>c(C2O42-)>c(HC2O4-)>c(OH-)>c(H+) |
分析 将0.1mol/L的NaHC2O4溶液与0.1mol/L的NaOH溶液等体积混合后,二者恰好完全反应生成0.05mol/L的 Na2C2O4,溶液中存在电荷守恒和物料守恒,据此分析解答.
解答 解:将0.1mol/L的NaHC2O4溶液与0.1mol/L的NaOH溶液等体积混合后,二者恰好完全反应生成0.05mol/L的 Na2C2O4,
A.溶液中存在电荷守恒,根据电荷守恒得c(Na+)+c(H+)=c(HC2O4-)+c (OH-)+2 c (C2O42-),故A正确;
B.溶液中存在物料守恒,根据物料守恒得c (Na+)=2[c(HC2O4-)+c(H2C2O4)+c(C2O42-)],故B正确;
C.电荷守恒得c(Na+)+c(H+)=c(HC2O4-)+c (OH-)+2 c (C2O42-),根据物料守恒得c (Na+)=2[c(HC2O4-)+c(H2C2O4)+c(C2O42-)],所以得c (OH-)-c(H+)=c(HC2O4-)+2 c (H2C2O4),故C正确;
D.钠离子不水解、草酸根离子水解但水解程度较小,草酸根离子两步水解都生成氢氧根离子,所以溶液中离子浓度大小顺序是c (Na+)>c (C2O42-)>c (OH-)>c(HC2O4-)>c(H+),故D错误;
故选D.
点评 本题考查离子浓度大小比较,为高频考点,侧重考查学生分析判断能力,明确溶液中溶质成分及其性质是解本题关键,任何电解质溶液中都存在电荷守恒、物料守恒,注意守恒思想的灵活运用,题目难度中等.


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:解答题
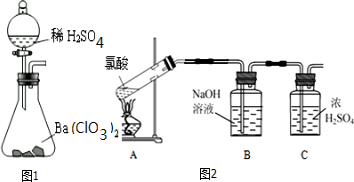
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若X和Y处于同一周期,则X的原子半径肯定小于Y的原子半径 | |
| B. | 若X和Y处于同一周期,且M属于共价化合物,则分子中原子个数比可能为1:2 | |
| C. | 若最外层电子数X>Y>2,则X的非金属性一定比Y的非金属性强 | |
| D. | 若M属于离子化合物,则该化合物中只存在离子键,且每个原子均达到8电子稳定结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X与Y形成化合物时,X可以显负价,Y显正价 | |
| B. | 在元素同周期表中X可能位于Y的右面 | |
| C. | 最高价含氧酸的酸性:X对应的酸性弱于Y对应的酸性 | |
| D. | Y的气态氢化物的稳定性小于X的气态氢化物的稳定性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 $→_{△}^{浓硫酸}$CH3COOCH(CH3)2+H2O.
$→_{△}^{浓硫酸}$CH3COOCH(CH3)2+H2O.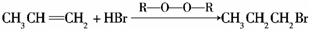 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
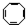 互为同分异构体且属于芳香烃的有机物的结构简式
互为同分异构体且属于芳香烃的有机物的结构简式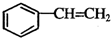 .
. 、
、 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2 NaOH NaCl MgO | B. | H2SO4 AlCl3 CaCO3 Na2O | ||
| C. | NO2 Ba(OH)2 CaO H2O2 | D. | HBr KOH BaSO4 CuO |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | CCl4和SiCl4的熔点 | B. | NH3与H2O的键角 | ||
| C. | SO2和CO2在水中的溶解度 | D. | 碳化硅和金刚石的硬度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 12C、13C、14C、石墨都是碳元素的同位素 | |
| B. | 同种元素的原子,质量数一定相同 | |
| C. | 互为同位素的原子,质子数一定相同 | |
| D. | 由一种元素组成的物质,一定是纯净物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com