
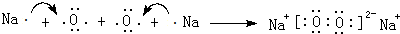 .
.分析 A、B、C、D、E、F六种短周期元素的原子序数依次增大,A能分别与B、C形成电子总数相等的分子,且A与C能形成两种常温下为液态的化合物,两种液态化合物为H2O、H2O2,可知A为H元素、C为O元素,A、B的最外层电子数之和与C的最外层电子数相等,则B为N元素,A与D、C与E同主族,D、E、F同周期,则D为Na、E为S、F为Cl,据此解答.
解答 解:A、B、C、D、E、F六种短周期元素的原子序数依次增大,A能分别与B、C形成电子总数相等的分子,且A与C能形成两种常温下为液态的化合物,两种液态化合物为H2O、H2O2,可知A为H元素、C为O元素,A、B的最外层电子数之和与C的最外层电子数相等,则B为N元素,A与D、C与E同主族,D、E、F同周期,则D为Na、E为S、F为Cl.
(1)D、E、F最高价氧化物对应水化物分别为NaOH、硫酸、高氯酸,氢氧化钠溶液呈碱性,硫酸、高氯酸为酸性,均为强酸,相同浓度时硫酸的酸性更强,故pH由大到小的顺序为:NaOH>HClO4>H2SO4,
故答案为:NaOH>HClO4>H2SO4;
(2)单质D在单质C中燃烧生成产物为Na2O2,用电子式表示其形成过程为: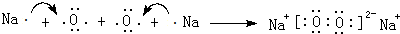 ,
,
故答案为: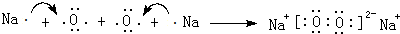 ;
;
(3)B与F两种元素形成一种化合物分子,分子中各原子均达到8电子稳定结构,该化合物为NCl3,能与水反应生成HClO和另一种常见的气态产物为氨气,该反应的化学方程式:NCl3+3H2O=NH3↑+3HClO,
故答案为:NCl3+3H2O=NH3↑+3HClO.
点评 本题考查结构性质与位置关系应用,推断元素是解题关键,注意掌握用电子式表示物质或化学键形成,(3)中利用水解原理理解发生的反应.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:多选题
| A. | Al2O3 | B. | H2SO3 | C. | H2S | D. | NaHCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化铝可用于治疗胃酸过多 | |
| B. | ClO2用于饮用水消毒 | |
| C. | 水玻璃浸泡过的木材既能防腐又能耐火 | |
| D. | Si用于制造光导纤维 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 增加Fe的物质的量 | |
| B. | 将容器的体积缩小一半 | |
| C. | 保持体积不变,充入水蒸气 | |
| D. | 压强不变,充入Ne使容器的体积增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 目的 | 试剂或试验方法 | 说明 |
| A | 从苯中提溴 | 加CCl4 | 溴易溶于CCl4 |
| B | 检验含Fe3+溶液中是否含Fe2+ | 加高锰酸钾溶液 | 溶液紫色褪去,说明含Fe2+ |
| C | 配置1mol/LFeCl3溶液100mL | 将一定质量FeCl3溶液转移至容量瓶中加水定容 | 容量瓶规格须为100mL |
| D | 制取漂白粉 | 将氯气通入澄清石灰水中 | 氯气与氢氧化钙反应生成次氯酸钙 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有①② | B. | 只有①③ | C. | 只有①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Kw(NH3•H2O) | B. | n(OH-) | C. | $\frac{c(N{H}_{3}•{H}_{2}O)}{c(O{H}^{-})}$ | D. | c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu2+ Fe2+ | B. | H+ | C. | Cu2+ Fe3+ | D. | Fe2+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com