
【题目】某温度下,在一个1L 的密闭容器中,X、Y、Z 三种气态物质的物质的量随时间的变化曲线如图所示。根据图中数据,填写下列空白:
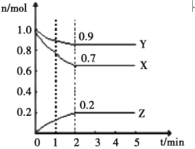
(1)2min时,Y 的物质的量浓度是____________;
(2)从开始至2min,X 的平均反应速率为_________;
(3)该反应的化学方程式为____________________;
(4)1min时,v(正)____v(逆),2min时,v(正)____v(逆) (填“>”或“<”或“=”);
(5)在2min时,向容器中通入氩气,增大体系压强,X 的化学反应速率将______;
(6)2min时,x的转化率为________。
【答案】0.9mo1L-1 0.15mo1L-1min-1 3X(g)+Y(g)2Z(g) > = 不变 30%
【解析】
由图可知,从反应开始到达到平衡,X、Y的物质的量减少,应为反应物,Z的物质的量增加,应为生成物,从反应开始到第2分钟反应到达平衡状态,X、Y消耗的物质的量分别为0.3 mol、0.1 mol,,Z的生成的物质的量为0.2 mol,物质的量的变化量之比为3: 1: 2,物质的量变化之比等于化学计量数之比,据此解答。
(1).由图可知:在2min时Y的物质的量为0.9mol,容器体积为1L,则Y的物质的量的浓度为:![]() ,故答案为:0.9mo1L-1;
,故答案为:0.9mo1L-1;
(2).从开始至2min,X的变化的物质的量为1mol -0.7mol=0.3mol,由公式:![]() ;故答案:0.15mo1L-1min-1;
;故答案:0.15mo1L-1min-1;
(3).由图可知,从反应开始到达到平衡,X、Y的物质的量减少,应为反应物,Z的物质的量增加,应为生成物,从反应开始到第2分钟反应到达平衡状态,X、Y消耗的物质的量分别为0.3 mol、0.1 mol,,Z的生成的物质的量为0.2 mol,物质的量的变化量之比为3: 1: 2,物质的量变化之比等于化学计量数之比,则化学方程式为3X(g)+Y(g)2Z(g),故答案为:3X(g)+Y(g)2Z(g);
(4).1min时,平衡正向进行,则正逆反应速率的大小关系为: v(正)>v (逆);2min时反应正好达到平衡,则正逆反应速率的大小关系为:V(正)=V(逆),故答案为:>;=;
(5).容器体积恒定,通入惰性气体氩气,对反应物浓度没有影响,故X的反应速率不变;故答案为:不变;
(6).![]() 则x的转化率=
则x的转化率=![]() ,故答案为:30%。
,故答案为:30%。


 计算高手系列答案
计算高手系列答案科目:高中化学 来源: 题型:
【题目】某同学为了验证碳和硅两种元素非金属性的相对强弱,用图示装置进行实验(夹持仪器已略去,气密性已检验)。

回答下列问题:
(1)仪器a的名称:___________________。
(2)打开弹簧夹1,关闭弹簧夹2,旋开仪器a的活塞滴加盐酸。一段时间后,A中现象是________;原因是________。
(3)关闭弹簧夹1,打开弹簧夹2,D中出现白色胶状沉淀,X是________(填化学式),D中发生反应的化学方程式是___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】a mL三种气态烃组成的混合物与足量氧气混合,点燃爆炸后,恢复到原来的状态(常温、常压),体积共缩小2a mL。则三种烃可能是( )
A.C2H4、C2H2、CH4B.C2H6、C3H6、C4H6
C.CH4、C2H6、C3H8D.CH4、C2H4、C3H4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,回答下列问题:
族 周期 | IA | 0 | ||||||
1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
2 | ② | ③ | ④ | |||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(1)①形成的阴离子的结构示意图为___。如果③原子中含8个中子,则其原子符号为___。
(2)③、④、⑤、⑥简单离子半径由小到大的顺序为___。(填离子符号)
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:___。
(4)设计实验证明⑧的非金属性比⑦强,用化学方程式表示___。
(5)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:
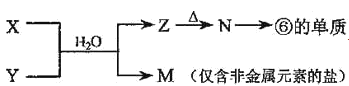
(a)X溶液与Y溶液反应的离子方程式为___。
(b)N→⑥的单质的化学方程式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ClO2是一种具有强氧化性的黄绿色气体,也是优良的消毒剂,熔点-59℃、沸点11℃,易溶于水,易与碱液反应。ClO2浓度大时易分解爆炸,在生产和使用时必须用稀有气体或空气等进行稀释,实验室常用下列方法制备:2NaC1O3+Na2SO3+H2SO4![]() 2C1O2↑+2Na2SO4+H2O。
2C1O2↑+2Na2SO4+H2O。
(1)H2C2O4可代替Na2SO3制备ClO2,该反应的化学方程式为___,该方法中最突出的优点是___。
(2)ClO2浓度过高时易发生分解,故常将其制备成NaClO2固体,以便运输和贮存。
已知:2NaOH+H2O2+2ClO2=2NaClO2+O2+2H2O,实验室模拟制备NaC1O2的装置如图所示(加热和夹持装置略)。
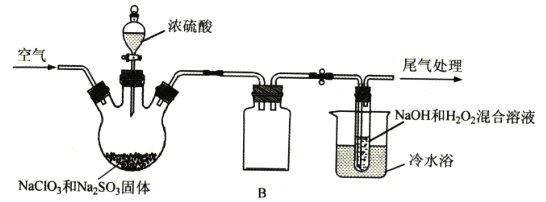
①产生ClO2的温度需要控制在50℃,应采取的加热方式是___;盛放浓硫酸的仪器为:___;NaC1O2的名称是___;
②仪器B的作用是___;冷水浴冷却的目的有___(任写两条);
③空气流速过快或过慢,均会降低NaC1O2的产率,试解释其原因___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苏合香醇可用作食用香精,其结构简式如图所示
![]()
(1)苏合香醇的分子式为________,它不能发生的有机反应类型有________(填数字序号)。
①取代反应 ②加成反应 ③消去反应
④加聚反应 ⑤氧化反应 ⑥还原反应
有机物丙是一种香料,其合成路线如下图。其中甲的相对分子质量通过质谱法测得为88,它的核磁共振氢谱显示只有三组峰;乙与苏合香醇互为同系物。
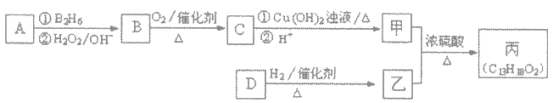
已知:![]()
![]()
![]()
(2)按照系统命名法,A的名称是_________。
(3)C与新制Cu(OH)2悬浊液反应的化学方程式为______。
(4)丙中含有两个-CH3,在催化剂存在下1mol D与2mol H2可以反应生成乙,且D可发生银镜反应,则D的结构简式为_____________。
(5)甲与乙反应的化学方程式为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机物1-氧杂-2,4-环戊二烯(![]() )的说法正确的是()
)的说法正确的是()
A.![]() 与
与![]() 互为同系物
互为同系物
B.一氯代物有2种,二氯代物有4种(不考虑立体异构)
C.能使溴水退色,不能使酸性高锰酸钾溶液退色
D.1mol该有机物完全燃烧消耗5molO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按下图装置进行实验,若![]() 轴表示流入正极的电子的物质的量,则y轴可以表示( )
轴表示流入正极的电子的物质的量,则y轴可以表示( )
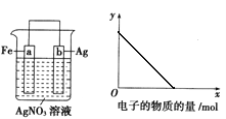
①c(Ag+) ②c(NO3-)③a棒的质量 ④b棒的质量 ⑤溶液的质量
A.①③ B.②④ C.①③⑤ D.②④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科研团队成功研究出高比能量、低成本的钠离子二次电池,其工作原理示意图如图。已知电池反应:Na1-xMnO2+NaxCn![]() NaMnO2+nC。下列说法正确的是( )
NaMnO2+nC。下列说法正确的是( )
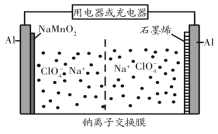
A.电池放电过程中,NaMnO2/Al上的电势低于石墨烯/Al上的电势
B.电池放电时,正极可发生反应Na1-xMnO2+xNa++xe-=NaMnO2
C.电池充电时,外接电源的负极连接NaMnO2/Al电极
D.电池充电时,Na+由NaMnO2/Al电极移向石墨烯/Al电极
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com