
| A. | 根据元素在周期表中的位置,推测元素的原子结构 | |
| B. | 指导新元素的发现和合成,预测新元素的性质 | |
| C. | 在金属与非金属的分界线附近寻找半导体材料 | |
| D. | 在零族元素中寻找耐腐蚀的金属材料 |
分析 A、原子核外电子层等于元素所在的周期表的周期数,原子核外最外层电子数等于所在族序数;
B.结合同周期、同族元素性质的相似性、递变性解答;
C、在金属与非金属的分界线附近寻找半导体材料;
D、在过渡元素中寻找耐腐蚀的金属材料.
解答 解:A、原子核外电子层等于元素所在的周期表的周期数,原子核外最外层电子数等于所在族序数,所以可以根据元素在周期表中的位置,推测元素的原子结构,故A正确;
B.同周期、同族元素性质具有一定相似性、递变性,位置靠近的元素性质相似,为新元素的发现和预测它们的原子结构和性质提供线索,故B正确;
C、在金属与非金属的分界线附近寻找半导体材料,故C正确;
D、在过渡元素中寻找耐腐蚀的金属材料,而不是零族元素,故D错误;
故选D.
点评 本题考查元素周期表与元素周期律的应用,题目较为简单,注意基础知识的积累.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:多选题
| 化学式 | AgCl | Ag2CrO4 | CH3COOH | H2CO3 | HClO |
| Ksp或Ka | Ksp=1.8×10-10 | Ksp=2×10-12 | Ka=1.8×10-5 | Ka1=4.3×10-7 Ka2=5.6×10-11 | Ka=3×10-8 |
| A. | lmolCl2通入足量的水中充分反应,转移的电子数约为6.02×1023 | |
| B. | 将少量CO2气体通入NaClO溶液中的离子方程式:CO2+H2O+ClO-═HCO3-+HC1O | |
| C. | 常温下,用蒸馏水不断稀释醋酸,溶液中$\frac{c(C{H}_{3}COOH)}{c({H}^{+})}$的值不变 | |
| D. | 向浓度均为1×103 mol/L-1的KC1和K2CrO4混合溶液中滴加1×10-3 mol/L-1的AgNO3溶液Cl-先沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | C | D | E |
| A. | HnDOm为强酸时,E的非金属性一定很强 | |
| B. | A(OH)n为强碱时,B(OH)m也一定为强碱 | |
| C. | E元素的最高化合价为+7时,D元素的负化合价可为-2价 | |
| D. | HnCOm为强酸时,E的单质可能有强还原性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 规律 | 结论 |
| A | 同主族元素性质的相似性 | 钠和氧反应可以形成Na2O2,也可以和硫形成Na2S2 |
| B | 反应物浓度越大,反应速率越快 | 常温下,相同的铁片分别加入足量的稀硫酸和浓硫酸中,浓硫酸中铁片先溶解完 |
| C | 结构和组成相似的物质,沸点随相对分子质量增大而升高 | H2O沸点低于H2S |
| D | 较强酸可以制取较弱酸 | 亚硫酸和次氯酸钙反应可以制取次氯酸 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷、乙烷、丙烷在光照下分别与氯气反应,生成的一氯代物都只有一种 | |
| B. | 利用减压过滤的方法可以用来快速分离、提纯蛋白质 | |
| C. | 苯与溴水混合,反复振荡后溴水层褪色,这是由于发生了取代反应 | |
| D. | 邻二甲苯只有一种结构,证明苯环中不存在碳碳单键和碳碳双键交替的结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
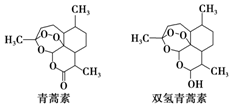 中国科学家屠呦呦因创制新型抗疟药--青蒿素和双氢青蒿素获得2015年诺贝尔生理学或医学奖.青蒿素和双氢青蒿素的结构式如图.从青蒿中提取青蒿素主要采用有机溶剂提取的方法.下列有关说法不正确的是( )
中国科学家屠呦呦因创制新型抗疟药--青蒿素和双氢青蒿素获得2015年诺贝尔生理学或医学奖.青蒿素和双氢青蒿素的结构式如图.从青蒿中提取青蒿素主要采用有机溶剂提取的方法.下列有关说法不正确的是( )| A. | 青蒿素的分子式为C15H22O5 | |
| B. | 青蒿素通过还原反应可制得双氢青蒿素 | |
| C. | 青蒿素有青蒿的芳香气味,是芳香族化合物 | |
| D. | 用有机溶剂乙醚从青蒿中提取青蒿素,主要采用萃取的方法 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 136.8kJ | B. | 110.9kJ | C. | 83.2kJ | D. | 82.4kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| X | Y | |
| Z | W |
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com