
【题目】下述实验中均有红棕色气体产生,对比分析所得结论正确的是( )
① | ② | ③ |
|
|
|
A.由①中的红棕色气体,可推知反应还有氧气产生
B.红棕色气体表明②中木炭与浓硝酸发生了反应
C.由③可说明浓硝酸具有挥发性和强氧化性
D.③的气体产物中检测出CO2,由此说明木炭一定与浓硝酸发生了反应
【答案】AC
【解析】
A.由①中的红棕色气体可知,该气体为NO2,由此可以推知:HNO3中+5价的N降低到+4价,发生还原反应,那么只有氧元素的化合价由-2价升高到0价,发生氧化反应,产生了氧气,故A正确;
B.浓硝酸与木炭加热时发生氧化还原反应,木炭被浓硝酸氧化生成二氧化碳,浓硝酸被还原成二氧化氮,二氧化氮气体为红棕色气体,但硝酸化学性质不稳定,见光或受热能分解,也会生成红棕色的二氧化氮气体,故B错误;
C.根据实验③,浓硝酸没有与木炭直接接触,若红棕色气体是硝酸分解生成的,那说明浓硝酸有挥发性,先挥发然后受热分解,若红棕色气体是木炭和浓硝酸反应生成的,也证明浓硝酸有挥发性,其次,无论红棕色气体是浓硝酸直接受热分解得到的,还是与木炭反应生成的,二氧化氮都是还原产物,可说明浓硝酸具有挥发性和强氧化性,故C正确;
D.③中红热的木炭在空气中也能生成二氧化碳,所以检测到二氧化碳并不能说明是木炭与浓硝酸发生了反应,故D错误;
故答案选AC。


 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案科目:高中化学 来源: 题型:
【题目】关于下列装置的说法正确的是
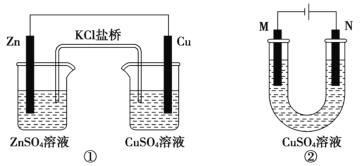
A.装置①将电能转变为化学能
B.装置①中盐桥内的 K+移向 CuSO4 溶液
C.若装置②用于铁棒镀铜,则 N 极为铁棒
D.若装置②用于电解精炼铜,溶液中的 Cu2+浓度保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年是元素周期表发表150周年,期间科学家为完善周期表做出了不懈努力。中国科学院院士张青莲教授曾主持测定了铟(49In)等9种元素相对原子质量的新值,被采用为国际新标准。铟与铷(37Rb)同周期。下列说法不正确的是
A. In是第五周期第ⅢA族元素
B. 11549In的中子数与电子数的差值为17
C. 原子半径:In>Al
D. 碱性:In(OH)3>RbOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有五种元素,其中A、B、C为短周期主族元素,D、E为第四周期元素,它们的原子序数依次增大。请根据下列相关信息回答问题:
A元素原子的核外电子数和电子层数相等
B元素原子的核外p电子数比s电子数少1
C元素的第一至第四电离能如下:![]()
![]()
![]()
![]()
D是前四周期中金属性最强的元素
E在周期表的第七列
(1)已知BA5为离子化合物,写出其电子式:__________。
(2)B元素基态原子中能量最高的电子,其电子云在空间有___个伸展方向,原子轨道呈 _____ 形。
(3)某同学根据上述信息,推断C元素基态原子的轨道表示式为 ,该同学所画的轨道表示式违背了 __________________ 。
,该同学所画的轨道表示式违背了 __________________ 。
(4)E位于第 _________ 族、 _____ 区,该元素原子的核外电子排布式为 _______。
(5)检验D元素的方法是 _____ ,请用原子结构的知识解释产生此现象的原因:__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容中发生下列反应aA(g)![]() cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述正确的是
cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述正确的是
A. A的转化率变小 B. 平衡向正反应方向移动
C. D的体积分数变大 D. a> c+d
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国航空航天事业飞速发展,银铜合金广泛用于航空工业。从银精矿(其化学成分有:Ag、Zn、Cu、Pb、S及SiO2等)中提取银、铜和铅,工艺流程如图所示。

(1)步骤①当盐酸的浓度和KClO3的量一定时,写出两点可提高“浸取”速率的措施______;从Cu和Pb混合物中提取Cu的试剂为______(填名称)。
(2)步骤③反应的化学方程式为______。
(3)步骤④分离出的滤渣中主要含有两种杂质,为了回收滤渣中的非金属单质,某实验小组向滤渣中加入试剂______(填化学式),充分溶解后过滤,然后将滤液进行______(填操作名称),得到该固体非金属单质。
(4)步骤⑤反应中氧化剂和还原剂的物质的量之比为______。
(5)排放后的废水中含有NO3-,任意排放会造成水体污染,科技人员在碱性条件下用Al粉将NO3-还原成无污染气体排放,该方法的缺点是处理后的水中生成了AlO2-,依然对人类健康有害。该反应的离子方程式为:______。25℃时,欲将上述处理过的水中的c(AlO2-)降到1.0×10-7mol/L,此时水中c(Al3+)=______molL-1.(已知,25℃,Ksp(Al(OH)3]=1.3×10-33,Al(OH)3(s)H++AlO2-+H2O,Ka=1.0×10-13)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用如图装置测定中和热的实验步骤如下:

①用量筒量取50 mL 0.25mol·L-1硫酸倒入小烧杯中,测出硫酸温度;
②用另一量筒量取50 mL 0.55mol·L-1NaOH溶液,并用另一温度计测出其温度;
③将NaOH溶液倒入小烧杯中,设法使之混合均匀,测出混合液最高温度。
回答下列问题:
(1)写出稀硫酸和稀氢氧化钠溶液反应表示中和热的热化学方程式(中和热数值为57.3kJ·mol-1)___________。
(2)倒入NaOH溶液的正确操作是__________(从下列选项中选出)。
A.沿玻璃棒缓慢倒入 B.分三次少量倒入 C.一次迅速倒入
(3)使硫酸与NaOH溶液混合均匀的正确操作是________(从下列选项中选出)。
A.用温度计小心搅拌
B.揭开硬纸片用玻璃棒搅拌
C.轻轻地振荡烧杯
D.用套在温度计上的环形玻璃搅拌棒轻轻地搅动
(4)实验数据如下表:
①请填写下表中的空白:
起始温度t1℃ | 终止温度t2/℃ | 温度差平均值(t2-t1)/℃ | |||
H2SO4 | NaOH | 平均值 | |||
1 | 26.2 | 26.0 | 26.1 | 29.5 | _____ |
2 | 27.0 | 27.4 | 27.2 | 32.3 | |
3 | 25.9 | 25.9 | 25.9 | 29.2 | |
4 | 26.4 | 26.2 | 26.3 | 29.8 | |
②近似认为0.55mol·L-1NaOH溶液和0.25mol·L-1硫酸溶液的密度都是1 g·cm-3,中和后生成溶液的比热容c=4.18 J·g-1·℃-1。则中和热ΔH=________(取小数点后一位)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】处理、回收利用CO是环境科学家研究的热点课题。回答下列问题:
Ⅰ.处理大气污染物
CO用于处理大气污染物N2O所发生的反应原理为:![]()
![]() 有人提出上述反应可以用“Fe+”作催化剂。
有人提出上述反应可以用“Fe+”作催化剂。
其总反应分两步进行:(1)第一步:![]() ;第二步:____ (写反应方程式)。
;第二步:____ (写反应方程式)。
(2)第二步反应不影响总反应达到平衡所用时间,由此推知,第二步反应速率____ 第一步反应速率(填“大于”“小于”或“等于”)。
Ⅱ.合成天然气(SNG)涉及的主要反应原理如下:
CO甲烷化: ![]()
![]()
水煤气变换: ![]()
![]()
(3)反应![]() 的△H= ___kJ/mol。
的△H= ___kJ/mol。
(4)在一恒容容器中,按照nmolCO和3nmolH2投料发生CO甲烷化反应,测得CO在不同温度下的平衡转化率与压强的关系如右图所示,下列说法正确的是_____(填标号)。

a.温度:T1<T2<T3
b.正反应速率:v(e)>v(c)>v(b)
c.平衡常数:K(a)<K(d)<K(c)
d.平均摩尔质量:M(a)>M(b)=M(e)
(5)在恒压管道反应器中,按n(H2)︰n(CO)=3︰1通入原料气发生CO甲烷化反应,400℃、P总为100kPa时反应体系平衡组成如下表所示。
组分 | H2 | CO | CH4 | H2O | CO2 |
体积分数 | 8.50 | 1.50 | 45.0 | 44.0 | 1.00 |
则该条件下CO的总转化率α= ___。 (保留一位小数)
(6)将制备的CH4用来组成下图所示燃料电池电解制备N2O5

①阳极的电极反应为_____。
②理论上制备1molN2O5,石墨2电极消耗气体的体积为_____L(标准状况)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某些共价键的键长数据如下表所示。试根据下表回答问题。
共价键 |
|
|
|
|
|
|
|
|
键长 | 0.154 | 0.134 | 0.121 | 0.143 | 0.123 | 0.146 | 0.122 | 0.110 |
(1)根据表中有关数据,你能推断出影响共价键键长的因素主要有哪些?_______。其影响的结果怎样?__________。
(2)通常,键能越__________,共价键越____,由该键构成的分子越稳定。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com