
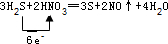 ��
������ ��2H2O+Cl2+SO2�TH2SO4+2HCl��ClԪ�صĻ��ϼ۽��ͣ�SԪ�صĻ��ϼ����ߣ�������Ϊ����������������Ϊ��ԭ����
��2KMnO4+16HCl�T2KCl+2MnCl2+5Cl2��+8H2O��MnԪ�صĻ��ϼ۽��ͣ�ClԪ�صĻ��ϼ����ߣ���������Ϊ��������HClΪ��ԭ�����Դ˽��1������3����
��4��H2S��HNO3�ɷ�Ӧ����S��NO��H2O��SԪ�صĻ��ϼ۽��ͣ�NԪ�صĻ��ϼ����ߣ�1mol���ᷴӦת��3mol���ӣ��Դ������
��� �⣺��2H2O+Cl2+SO2�TH2SO4+2HCl��ClԪ�صĻ��ϼ۽��ͣ�SԪ�صĻ��ϼ����ߣ�������Ϊ����������������Ϊ��ԭ����
��2KMnO4+16HCl�T2KCl+2MnCl2+5Cl2��+8H2O��MnԪ�صĻ��ϼ۽��ͣ�ClԪ�صĻ��ϼ����ߣ���������Ϊ��������HClΪ��ԭ����
��1�����������������Դ�����������������Կ�֪����������������ǿ��˳��ΪKMnO4��Cl2����ԭ���Ļ�ԭ�Դ��ڻ�ԭ����Ļ�ԭ�Կ�֪����ԭ���Ļ�ԭ��ǿ��˳��ΪSO2��HCl��
�ʴ�Ϊ��KMnO4��Cl2��SO2��HCl����
��2����Ӧ�����������H2SO4���ͻ�ԭ���HCl��������Ϊ98��73���ʴ�Ϊ��98��73��
��3�������������ֻ�ԭ�ԣ��������������ԣ���Ӧ�����Ȼ�����ֳ���������a��b���ʴ�Ϊ��a��b��
��4��H2S��HNO3�ɷ�Ӧ����S��NO��H2O��5�����ʷ���3H2S+2HNO3�T3S+2NO��+4H2O��
��Sʧȥ���ӣ�N�õ����ӣ��÷�Ӧ��ת��6e-������ת�Ƶķ������ĿΪ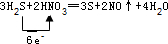
 ���ʴ�Ϊ��
���ʴ�Ϊ��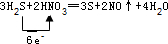 ��
��
��SԪ�صĻ��ϼ����ߣ���H2SΪ��ԭ����NԪ�صĻ��ϼ۽��ͣ��õ����ӱ���ԭ����ԭ����ΪNO��
�ʴ�Ϊ��H2S��NO��
��ת��6mol��������4molˮ����ת����0.3mol���ӣ�������ˮ��������0.3mol��$\frac{4}{6}$��18g/mol=3.6g��
�ʴ�Ϊ��3.6g��
���� ���⿼��������ԭ��Ӧ��Ϊ��Ƶ���㣬���շ�Ӧ��Ԫ�صĻ��ϼ۱仯Ϊ���Ĺؼ������ط�����Ӧ�������Ŀ��飬ע�����ת�Ƶı�ʾ��������Ŀ�ѶȲ���


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
 ����0.02500mol/L�ı�������Һ�ζ�ijδ֪Ũ�ȵ�����������Һ���й����ݼ�¼�����
����0.02500mol/L�ı�������Һ�ζ�ijδ֪Ũ�ȵ�����������Һ���й����ݼ�¼�����| ��� | ����Һ�����ml�� | �����ı�����������ml�� | ||
| �ζ�ǰ | �ζ��� | ������� | ||
| 1 | 25.00 | 1.00 | 27.30 | 26.30 |
| 2 | 25.00 | �� | �� | �� |
| 3 | 25.00 | 1.50 | 27.84 | 26.34 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
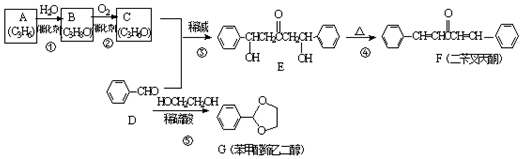
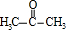 ��A�Ӿ۲���Ľṹ��ʽ��
��A�Ӿ۲���Ľṹ��ʽ��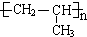 ��
��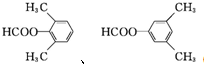 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
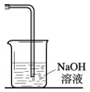 ʵ���ҳ������·�����ȡ������MnO2+4HCl��Ũ�� $\frac{\underline{\;\;��\;\;}}{\;}$ MnCl2+Cl2��+2H2O��������һ����Ҫ�Ļ���ԭ�ϣ��ڹ�ũҵ������������������Ҫ��Ӧ�ã����������ѧ֪ʶ�ش�
ʵ���ҳ������·�����ȡ������MnO2+4HCl��Ũ�� $\frac{\underline{\;\;��\;\;}}{\;}$ MnCl2+Cl2��+2H2O��������һ����Ҫ�Ļ���ԭ�ϣ��ڹ�ũҵ������������������Ҫ��Ӧ�ã����������ѧ֪ʶ�ش��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���� | B�� | ���� | C�� | ���� | D�� | ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com