
分析 (1)MgCl2溶液中加入NaOH溶液,会生成白色的Mg(OH)2沉淀,据此书写离子方程式;向Mg(OH)2沉淀中加入FeCl3溶液,能发生沉淀的转化;
(2)A、为使离子完全沉淀,加入过量的沉淀剂,能使离子沉淀完全;
B、氢氧化铝是难溶物质,存在沉淀溶解平衡和电离平衡;
C、物质的溶解度不一定随温度的升高而增大;
D、Mg(OH)2的溶解度比MgCO3小.
解答 解:(1)MgCl2溶液中加入NaOH溶液,会生成白色的Mg(OH)2沉淀,离子方程式为:Mg2++2OH-=Mg(OH)2↓;
向Mg(OH)2沉淀中加入FeCl3溶液,能发生沉淀的转化,由白色的Mg(OH)2沉淀转化为红褐色的Fe(OH)3沉淀,离子方程式为:3Mg(OH)2+2Fe3+=2Fe(OH)3+3Mg2+;
故答案为:生成白色沉淀;Mg2++2OH-=Mg(OH)2↓;白色沉淀变为红褐色;3Mg(OH)2+2Fe3+=2Fe(OH)3+3Mg2+;
(2)A、为使离子完全沉淀,加入过量的沉淀剂,能使离子沉淀完全,故A正确;
B、氢氧化铝是难溶物质,存在沉淀溶解平衡和电离平衡,故B正确;
C、物质的溶解度不一定随温度的升高而增大,如氢氧化钙溶液随温度的升高溶解度减小,故D错误;
D、除去溶液中的Mg2+,用OH-比用CO32-效果好,说明Mg(OH)2的溶解度比MgCO3小,故D错误;
故选CD.
点评 本题考查较为综合,涉及沉淀溶解平衡的计算应用,难溶物质的溶解度比较方法,题目难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:推断题
| ① | ||||||
| ② | ③ | ④ | ||||
| ⑤ | ⑥ | ⑦ | ⑧ |
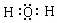 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
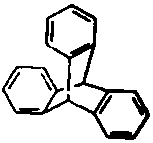
| A. | 三蝶烯是苯的同系物 | |
| B. | 三蝶烯能发生取代反应 | |
| C. | 三蝶烯的一氯代物有6种 | |
| D. | 三蝶烯分子中所有原子可能在同一平面上 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
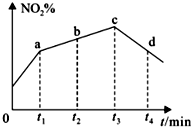 研究氧化物与悬浮在大气中的海盐粒子的相互作用时,涉及如下反应:
研究氧化物与悬浮在大气中的海盐粒子的相互作用时,涉及如下反应:查看答案和解析>>
科目:高中化学 来源: 题型:实验题
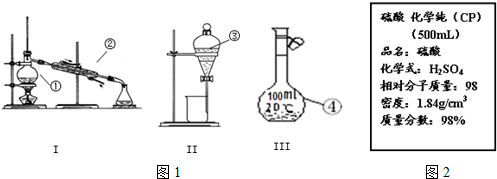
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 250mL2mol•L-1的氨水中含有NH3•H2O的分子数为0.5NA | |
| B. | 0.1 mol铁在0.1 mol Cl2中充分燃烧,转移的电子数为0.2 NA | |
| C. | 1 L 0.5 mol•L-1 Na2CO3溶液中含有的CO32-数为0.5NA | |
| D. | t℃时,pH=6 的纯水中含有OH-的个数为10-6NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com