
��10�֣����ֶ�����Ԫ�������ڱ��е����λ��������ʾ������ZԪ������������������Ӳ�����2������ش��������⣺
X | Y | |
Z | W |
��1��Ԫ��Zλ�����ڱ��е�λ��______________________��
��2��ʵ������ȡXԪ�ص��⻯��Ļ�ѧ����ʽΪ___________________________��
��3��W��Z������������Ӧ�ĺ����������____________��____________���û�ѧʽ��ʾ����
��4����W�ĵ���ͨ�뺬�����ʵ���FeBr2����Һ�У�������Ӧ�����ӷ���ʽΪ_________________��
��5��Z��X�γɵ�һ�ֻ�������Է���������170��190֮�䣬��Z����������ԼΪ70%���û�����Ļ�ѧʽΪ_____________________________��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2016�������ʡ������ѧ�����в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��a g�������̷�ĩ����b mol/L��Ũ����c L�м�����ȫ�ܽ⣬��Ӧ��ת�Ƶ���d������NAΪ�����ӵ�������ֵ������������ȷ����
A�������ռ�������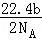 L
L
B����Ӧ����Һ�е�Cl����ĿΪ��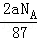
C��NA�ɱ�ʾΪ��
D����Ӧ����Һ�е�H+��ĿΪ��bc��2d
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�������˫Ѽɽ��һ��ѧ������ѧ�����в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����йػ�ѧ�����ʾ��ȷ����
A����������ķ���ʽ��SiO2
B������״̬��������صĵ��뷽��ʽ��KHSO4  K++HSO4-
K++HSO4-
C�����ĵ���ʽ��
D. HClO�Ľṹʽ��H��Cl��O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�������и�����ѧ��9���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
NAΪ�����ӵ���������ֵ������˵����ȷ����
A��7.2g CaO2�����������Ӻ�����������Ϊ0.3NA
B����Ӧ3H2��g����N2��g��  2NH3��g����H����92 kJ/mol�ų�����9.2kJʱ��ת�Ƶ���0.6NA
2NH3��g����H����92 kJ/mol�ų�����9.2kJʱ��ת�Ƶ���0.6NA
C��0.1 mol/L NH4Cl��Һ��Cl-������ĿΪ0.1NA
D��0.1 mol H2O2�����к����Թ��ۼ���ĿΪ0.3NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�걱����ѧ������ѧ��У��һ�ϳ鿼��ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵����ȷ����
A���Ȼ����Ħ������Ϊ 36.5g
B��1molH2SO4������Ϊ98 g��mol-1
C���κ����ʵ�Ħ������������������Է������������ԭ������
D��CO2��Ħ��������H2��Ħ��������22��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016��ӱ�ʡ������ѧ�����в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
0.6mol/L��Fe2��SO4��3��1.2mol/L��CuSO4�Ļ����Һ200mL������һ�������۳�ַ�Ӧ�����Һ��Fe2+��Cu2+���ʵ���֮��Ϊ2��1����������۵����ʵ���Ϊ
A��0.16 mol B��0.22mol C��0.30mol D��0.48mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016��ӱ�ʡ������ѧ�����в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
���й���Cl��N��S�ȷǽ���Ԫ�ص��ʼ��仯�����˵����ȷ����
A��Ư�۵ijɷ��Ǵ������
B��ʵ���ҿ���Ũ�����������
C����Ũ��ˮ�ε��������ƹ����п�����ȡ����
D������������������������Ӧ���ɵIJ����У����Ļ��ϼ���ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ���Ĵ�ʡ�˱��и߶���ѧ�����в��Ի�ѧ�Ծ��������棩 ���ͣ�ʵ����
Ϊ�ⶨijH2C2O4��Һ��Ũ�ȣ�ȡ����Һ����ƿ�У���������ϡH2SO4����Ũ��Ϊc mol/L KMnO4����Һ�ζ���
��1���ζ�ԭ��Ϊ��__________________________�������ӷ���ʽ��ʾ����
��2���ζ�ʱ��KMnO4��ҺӦװ�� �����ʽ����ʽ�����ζ����У��ﵽ�ζ��յ�ʱ������Ϊ ��
��3����ͼ��ʾ50mL�ζ�����Һ���λ�ã���ʱ�ζ�����Һ��Ķ���Ϊ____ mL��

��4��Ϊ�˼�Сʵ������ͬѧһ������������ʵ�飬����ÿ����ȡH2C2O4��Һ�����ΪVmL������ʵ������¼���£�
ʵ����� | ��һ�� | �ڶ��� | ������ |
����KMnO4��Һ���/mL | 26.32 | 25.35 | 25.30 |
���ϱ����Կ�������һ��ʵ���м�¼����KMnO4��Һ��������Զ��ں����Σ���ԭ�������
A��ʵ�����ʱ���ӿ̶��߶�ȡ�ζ��յ�ʱKMnO4��Һ�����
B���ζ�ǰ�ζ��ܼ��������ݣ��ζ�����������
C����һ�εζ�ʢװ��Һ�ĵζ���װҺǰ������ˮ��ϴ����δ�ñ�Һ��ϴ�������ξ��ñ�Һ��ϴ
D����һ�εζ��õ���ƿ�ô�װҺ��ϴ����������δ��ϴ
E���μ�KMnO4��Һ���죬δ������տ�����Һ��ɫ������ֹͣ�ζ�
��5�������������ݣ�д������H2C2O4�����ʵ���Ũ�ȵı���ʽ�����ػ���C= mol/L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�������и߶���ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
ij�¶��£�H2(g)��CO2(g)  H2O(g)��CO(g)��ƽ�ⳣ��K��
H2O(g)��CO(g)��ƽ�ⳣ��K��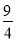 �����¶����ڼס��ҡ������������ܱ������У�Ͷ��H2(g)��CO2(g)������ʼŨ�������ʾ�������жϲ���ȷ����
�����¶����ڼס��ҡ������������ܱ������У�Ͷ��H2(g)��CO2(g)������ʼŨ�������ʾ�������жϲ���ȷ����
��ʼŨ�� | �� | �� | �� |
c(H2)(mol��L��1) | 0.010 | 0.020 | 0.020 |
c(CO2)(mol��L��1) | 0.010 | 0.010 | 0.020 |
A��ƽ��ʱ������CO2��ת���ʴ���60%
B��ƽ��ʱ�����кͱ���H2��ת���ʾ���60%
C��ƽ��ʱ������c(CO2)�Ǽ��е�2������0.012 mol��L��1
D����Ӧ��ʼʱ�����ķ�Ӧ������죬�ķ�Ӧ��������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com