
樱桃是一种抗氧化的水果,对人体有很大的益处,樱桃中含有一种羟基酸,具有健脾作用。下列有关说法正确的是
A.该羟基酸含有3种官能团
B.通常条件下,该羟基酸可以发生取代、氧化和加成反应
C.该羟基酸可以在Cu的催化下被O2氧化成醛
D.含1mol该羟基酸的溶液可与含2mol氢氧化钠的溶液恰好完全反应
科目:高中化学 来源: 题型:
所示装置中,观察到电流计指针偏转;M棒变粗;N棒变细。由此判断表中所列M、N、P物质,其中可以成立的是( )

| 选项 | M | N | P |
| A | Zn | Cu | 稀H2SO4溶液 |
| B | Cu | Fe | 稀HCl溶液 |
| C | Ag | Zn | AgNO3溶液 |
| D | Zn | Fe | FeSO4溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:H2(g)+F2(g) === 2HF(g) △H=-270kJ/mol,下列说法正确的是( )
A.1个氢气分子与1个氟气分子反应生成2个氟化氢分子放出270kJ
B.1mol氢气与1mol氟气反应生成2mol液态氟化氢放出的热量小于270kJ
C.在相同条件下,1mol氢气与1mol氟气的能量总和大于2mol氟化氢气体的能量
D.2mol氟化氢气体分解成1mol的氢气和1mol的氟气放出270kJ热量
查看答案和解析>>
科目:高中化学 来源: 题型:
容器中如下反应:X2(g)+Y2(g)  2Z(g),已知X2、Y2、Z的起始浓度分别为0.1mol/L、0.3mol/L、0.2mol/L,在一定条件下,当反应达到平衡时,各物质的浓度有可能是 ( )
2Z(g),已知X2、Y2、Z的起始浓度分别为0.1mol/L、0.3mol/L、0.2mol/L,在一定条件下,当反应达到平衡时,各物质的浓度有可能是 ( )
A.X2为0.2mol/L B.Y2为0.4mol/L C. Z为0.3mol/L D. Z为0.4mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
 中和热是指酸跟碱发生中和反应生成lmol H2O所放出的热量。某学生想通过测定反应过程中所放出的热量来计算中和热。他将50mL0.5mol/L的盐酸与50mL0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应。请回答下列问题:
中和热是指酸跟碱发生中和反应生成lmol H2O所放出的热量。某学生想通过测定反应过程中所放出的热量来计算中和热。他将50mL0.5mol/L的盐酸与50mL0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应。请回答下列问题:
(1) 从实验装置上看,图中尚缺少的一种玻璃用品是__________________,烧杯间填满碎塑料泡沫的作用是________________________________。
(2) 大烧杯上如不盖硬纸板,则求得的中和热数值_________(填“偏大”、“偏小’、“无影响”) (3) 实验中改用60 mL 0.50 mol/L的盐酸跟50mL 0.55 mol/L的NaOH溶液进行反应,上述实验相比,所放出的热量________(填“相等”或“不相等”),所求中和热的数值________(填“相等”或“不相等”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
有A、B、C、D、E五种常见化合物,都是由下表中的离子形成的:
| 阳离子 | K+ Na+ Cu2+ Al3+ |
| 阴离子 |
|
为了鉴别上述化合物,分别完成以下实验,其结果是:
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;
②将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀溶解;
③进行焰色反应,仅有B为紫色(透过蓝色钴玻璃);
④在各溶液中加入硝酸酸化的硝酸钡溶 液,只
液,只 有A中放出无色气体,只有D中产生白色沉淀;
有A中放出无色气体,只有D中产生白色沉淀;
⑤将B、C两溶液混合,未见沉淀或气体生成。根据上述实验填空:
(1)写出B、D的化学式:B ___,D 。
(2)C可用作净水剂,用离子方程式表示其净水原理______________。
(3)将含0.01 mol A的溶液与含0.02 mol E的溶液反应后, 向溶液中滴加0.1 mol·L-1稀盐酸。下列图象能正确表示加入盐酸的体积和生成CO2的物质的量的关系的是


(4)在m mL b mol·L-1 C溶液中,加入等体积a mol·L-1 的E溶液。
当a≤3b时,生成沉淀的物质的量是 mol;
当3b<a<4b时,生成沉淀的物质的量是 mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列表示物质结构的化学用语或模型中,正确的是
A.过氧化钠的电子式: B. S2-离子的结构示意图:
B. S2-离子的结构示意图:
C. 8个中子的碳原子的核素符号: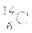 D. CH4分子的球棍模型:
D. CH4分子的球棍模型:
查看答案和解析>>
科目:高中化学 来源: 题型:
作为国家正在实施的“西气东输”工程终点站,上海将逐步改变以煤、石油为主的能源结构,这对解决城市环境污染意义重大。目前,上海大部分城市居民所使用的燃料主要是管道煤气,浦东新区居民开始使用东海天然气作为民用燃料。管道煤气的主要成分是CO、H2和少量烃类,天然气的主要成分是CH4,它们的燃烧反应如下:
2CO+O2 2CO2
2CO2
2H2+O2 2H2O
2H2O
CH4+2O2 CO2+2H2O
CO2+2H2O
根据以上化学方程式判断:燃烧相同体积的管道煤气和天然气,消耗空气体积较大的是________,因此燃烧管道煤气的灶具如需改烧天然气,灶具的改进方法是________进风口(填“增大”或“减小”),如不做改进,可能产生的不良后果是_____________。
管道煤气中含有烃类,除甲烷之外,还有少量乙烷、丙烷、丁烷等,它们的某些性质见下表。
| 乙烷 | 丙烷 | 丁烷 | |
| 烷点/℃ | -183.3 | -189.7 | -138.4 |
| 沸点/℃ | -88.6 | -42.1 | -0.5 |
试根据表中某个关键数据解释:冬天严寒季节有时管道煤气火焰很小,并且呈断续状态的原因是______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D是分布在三个不同短周期内除稀有气体以外的四种元素,它们的原子序数依次递增。已知B、D两种元素原子的最外层电子数是最内层电子数的两倍,而C元素原子的最外层电子数等于B元素原子的核外电子数。回答下列问题。
(1)画出C元素的原子结构示意图________。
(2)在化合物DC2的晶体结构中,最小的环上有________个D原子。
(3)在化合物BC2的晶体中,每个BC2分子周围与它距离最近的BC2分子有________个。
(4)写出符合通式BnAn(n≥6)且分子中所有A、B原子处于同一平面内的两种化合物的结构简式____________、____________。
(5)化合物DA4具有强还原性,将它加入硝酸银溶液中,会产生银镜,同时生成DC2和硝酸,该反应的化学方程式(用具体的化学式表示)是________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com