
| A.在氧化还原反应中,甲得电子比乙得电子多 |
| B.甲的最高价氧化物对应水化物酸性比乙的的最高价氧化物对应水化物酸性强 |
| C.甲的氢化物水溶液酸性比乙的氢化物水溶液酸性强 |
| D.向含甲和乙的阴离子的钠盐混合溶液中通入氯气,乙的阴离子先反应 |


科目:高中化学 来源:不详 题型:填空题
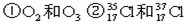 ③H2O和 D2O
③H2O和 D2O查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.晶格能: XCO3>YCO3 | B.阳离子半径: X2+>Y2+ |
| C.金属性: X>Y | D.氧化物的熔点: XO>YO |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.铍(Be)是一种金属,它的最高价氧化物的水化物可能具有两性 |
| B.砹是一种有色固体,HAt不稳定,AgAt是有色难溶于水的固体 |
| C.硫酸锶(SrSO4)是难溶于水和盐酸的白色固体 |
| D.硒化氢(H2Se)是无色、有毒、比H2S稳定的气体 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
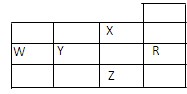
| A.W元素的第一电离能小于Y元素的第一电离能 |
| B.Y、Z的阴离子电子层结构都与R原子的相同 |
| C.最高价含氧酸的酸性,Y对应的酸性强于W |
| D.P能级未成对电子最多的是Z元素 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com