
【题目】一定条件下,H2O2在水溶液中发生分解反应:2H2O2 ![]() 2H2O + O2↑反应过程中,测得不同时间H2O2的物质的量浓度如下表:
2H2O + O2↑反应过程中,测得不同时间H2O2的物质的量浓度如下表:
![]()
(1)H2O2的分解反应__氧化还原反应(填“是”或“不是”)。要加快该反应的速率,可采取的方法有 。
(2)该分解反应0─20min的平均反应速率v(H2O2)为 mol·L-1 min-1。
(3)如果反应所用的H2O2溶液为100mL,则共产生O2 g。
A.0.08 B.0.16 C.1.2 D.2.4
【答案】(1)是;升高温度、使用催化剂、增加H2O2的浓度(2)0.02 ;(3)1.28
【解析】
试题分析:(1)H2O2的分解反应中氧元素化合价部分升高到0价,部分降低到-2价,属于氧化还原反应;要加快该反应的速率,可采取的方法有升高温度、使用催化剂、增加H2O2的浓度等。
(2)该分解反应0─20min双氧水的浓度减少0.80mol/L-0.40mol/L=0.4mol/L,因此双氧水的平均反应速率v(H2O2)=0.40mol/L÷20min=0.02mol·L-1 min-1。
(3)如果反应所用的H2O2溶液为100mL,物质的量是0.1L×0.8mol/L=0.08mol,根据方程式可知生成氧气是0.04mol,质量=0.04mol×32g/mol=1.28g。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】科学家最近研制出可望成为高效火箭推进剂的 N(NO2)3,如图:![]() 。已知该分子中 N-N-N 键角都是 108.1°,下列有关N(NO2)3的说法不正确的是( )
。已知该分子中 N-N-N 键角都是 108.1°,下列有关N(NO2)3的说法不正确的是( )
A.分子中 N、O 间形成的共价键是极性键
B.图中加“*”N原子的杂化方式为sp3
C.该物质既有氧化性又有还原性
D.15.2g 该物质含有 6.02×1022个原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化钙(CaO2·8H2O)是一种在水产养殖中广泛使用的供氧剂。
(3)水中溶解氧的测定方法如下:向一定量水样中加入适量MnSO4和碱性KI溶液,生成MnO(OH)2沉淀,密封静置;加入适量稀H2SO4,待MnO(OH)2与I完全反应生成Mn2+和I2后,以淀粉作指示剂,用Na2S2O3标准溶液滴定至终点,测定过程中物质的转化关系如下:
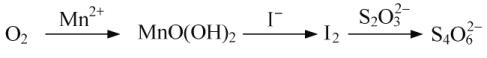
①写出O2将Mn2+氧化成MnO(OH)2的离子方程式;_____________。
②取加过一定量CaO2·8H2O的池塘水样100.00 mL,按上述方法测定水中溶解氧量,消耗0.01000 mol·L1 Na2S2O3标准溶液13.50 mL。计算该水样中的溶解氧(用mg·L1表示),写出计算过程。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 (NH4)2SO4是常见的化肥和化工原料,受热易分解。某兴趣小组拟探究其分解产物。
[查阅资料] (NH4)2SO4在260℃和400℃时分解产物不同。
[实验探究]该小组拟选用下图所示装置进行实验(夹持和加热装置略)
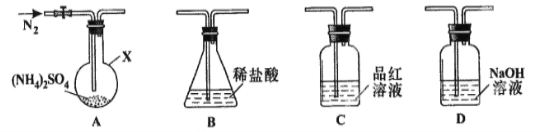
实验1:连接装置A-B-C-D,检查气密性,按图示加入试剂(装置B盛0.5000mol/L盐酸70.00mL)。通入N2排尽空气后,于260℃加热装置A一段时间,停止加热,冷却,停止通入N2,品红溶液不褪色。已知中和装置B中剩余盐酸需0.2000mol/L NaOH溶液25.00 mL,且中和后的溶液中无SO42-。
(1)仪器X的名称是________________;
(2)装置B内溶液吸收气体的物质的量是__________mol;
实验2:连接装置A-D-B,检查气密性,按图示重新加入试剂。通入N2排尽空气后,于400℃加热装置A至(NH4)2SO4完全分解无残留物,停止加热,冷却,停止通入N2。观察到装置A、D之间的导气管内有少量白色固体。经检验,该白色固体和装置D内溶液中有SO32-,无SO42-。进一步研究发现,气体产物中无氮氧化物。
(3)检验装置D内溶液中有SO32-,无SO42-的实验操作和现象是 ;
(4)装置B内溶液吸收的气体是 ;
(5)(NH4)2SO4在400℃分解的化学方程式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学在生活中有着广泛的应用,下列对应关系错误的是
化学性质 | 实际应用 | |
A. | Al2(SO4)3和小苏打反应 | 泡沫灭火器灭火 |
B. | 铁比铜金属性强 | Fe腐蚀Cu刻制印刷电路板 |
C. | 次氯酸盐具有氧化性 | 漂白粉漂白织物 |
D. | HF与SiO2反应 | 氢氟酸在玻璃器皿上刻蚀标记 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组元素性质或原子结构的递变,叙述不正确的是( )
A. Na、Mg、Al原子最外层电子数依次增多
B. P、S、Cl元素最高正化合价依次增大
C. N、O、F得电子能力依次减弱
D. LiOH、NaOH、KOH的碱性逐渐增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上曾经通过反应“3Fe+4NaOH![]() Fe3O4+2H2↑+4Na↑”生产金属钠。下列有关说法正确的是( )
Fe3O4+2H2↑+4Na↑”生产金属钠。下列有关说法正确的是( )
A.用磁铁可以将Fe与Fe3O4分离
B.将生成的气体在空气中冷却可获得钠
C.该反应条件下铁的氧化性比钠强
D.每生成1molH2,转移的电子数约为4×6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机化合物A含碳77.8%,氢7.40%,其余为氧,A的相对分子质量为甲烷的6.75倍。
(1)试计算确定该有机物的分子式(写出简明计算过程)。
(2)红外光谱测定,A分子结构中含有苯环和羟基。在常温下A可与浓溴水反应,1mol A最多可与2 molBr2作用,据此确定该有机物可能的结构简式。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com