
A、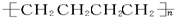 |
B、 |
C、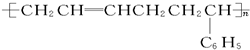 |
D、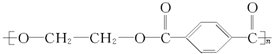 |
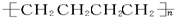 是加聚产物,其单体为CH2=CH2,不符合题意,故A错误;
是加聚产物,其单体为CH2=CH2,不符合题意,故A错误; 是加聚产物,其单体为CH2=CHCH=CH2,不符合题意,故B错误;
是加聚产物,其单体为CH2=CHCH=CH2,不符合题意,故B错误;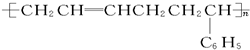 是加聚产物,其单体为CH2=CHCH=CH2和苯乙烯,符合题意,故C正确;
是加聚产物,其单体为CH2=CHCH=CH2和苯乙烯,符合题意,故C正确; 是缩聚产物,其单体是乙二醇和对苯二甲酸,不符合题意,故D错误;
是缩聚产物,其单体是乙二醇和对苯二甲酸,不符合题意,故D错误;

科目:高中化学 来源: 题型:
| A、与足量H2O反应,生成O2分子数目为0.1 NA |
| B、其中所含离子总数目为0.4NA |
| C、与足量CO2反应,转移的电子数目为0.1 NA |
| D、其中所含电子总数目为0.4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol氧单质一定含有2NA个氧原子 |
| B、含4mol C-O键的二氧化碳分子中含氧原子数为4NA |
| C、6.8g液态KHSO4中含有0.05NA个阳离子 |
| D、1molH3O+中含质子数为10NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 常温下 |
| SO2 |
| A、MFe2Ox是氧化剂 |
| B、x<y |
| C、SO2是该反应的催化剂 |
| D、SO2发生氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、① | B、②⑤ | C、①④ | D、①④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
| ||
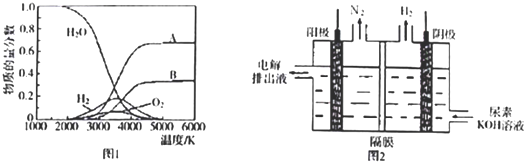

查看答案和解析>>
科目:高中化学 来源: 题型:
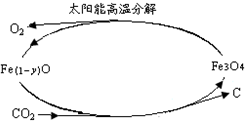 近年来,化学工作者在CO2的应用研究上取得了一些重要成果.
近年来,化学工作者在CO2的应用研究上取得了一些重要成果.| 3 |
| 2 |
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
| ||
| ||
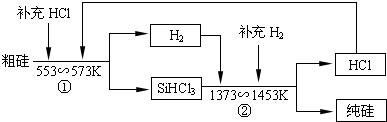
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com