
| A、68.76kJ |
| B、57.30 kJ |
| C、34.38kJ |
| D、17.19 kJ |


 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案科目:高中化学 来源: 题型:
| A、950 mL、201.4 g |
| B、1000 mL、212 g |
| C、任意规格、201.4 g |
| D、1000 mL、201.4 g |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | Si有良好的半导体性能 | Si可用于制备光导纤维 |
| B | SO2有漂白性 | SO2能使溴水褪色 |
| C | 浓硝酸有强氧化性 | 常温下可用铝罐储存浓硝酸 |
| D | 浓硫酸有吸水性 | 浓硫酸可用于干燥H2和CO |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、“硫黄姜”又黄又亮,可能是在用硫黄熏制的过程中产生的SO2所致 |
| B、天然纤维和人造纤维的主要成分都是纤维素 |
| C、发泡塑料饭盒主要材质是高分子材料,不适于盛放含油较多的食品 |
| D、NaHCO3能与酸反应,因此食品工业用小苏打做焙制糕点的膨松剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1、6 | B、2、7 |
| C、2、6 | D、1、7 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、酸a的浓度可能大于b |
| B、酸a的浓度可能等于b |
| C、酸a的酸性比醋酸弱 |
| D、酸a可能是强酸可能是弱酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
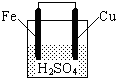
| A、铁棒是负极,发生氧化反应 |
| B、铜棒上有气体放出 |
| C、稀硫酸的pH值不断减小 |
| D、电池总反应方程式可表示为:Fe+2H+=Fe2++H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
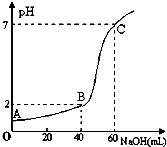 常温下,取20mL某浓度的HCl作为待测液,用一定物质的量浓度的NaOH溶液进行滴定(假设盐酸与NaOH溶液混合后体积变化忽略不计),滴定过程中溶液的pH变化如图所示.下列叙述正确的是( )
常温下,取20mL某浓度的HCl作为待测液,用一定物质的量浓度的NaOH溶液进行滴定(假设盐酸与NaOH溶液混合后体积变化忽略不计),滴定过程中溶液的pH变化如图所示.下列叙述正确的是( )| A、所用HCl的浓度是0.09mol?L-1,NaOH溶液浓度为0.03mol?L-1 |
| B、在B点,溶液中离子浓度关系为:c(Cl-)>c(Na+)>c(OH-)>c(H+) |
| C、A、B、C三点水的电离程度大小依次为:A>B>C |
| D、滴定前,锥形瓶用待测液润洗,导致HCl浓度偏低 |
查看答案和解析>>
科目:高中化学 来源: 题型:
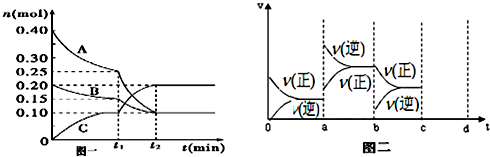
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com