
下列离子方程式书写正确的是( )
A.已知电离常数H2SO3;K1=1.3×10-2;K2=6.3×10-8;
H2CO3;K1=4.2×10-7;K2=5.6×10-11。
H2SO3溶液和NaHCO3溶液反应:H2SO3+2HCO3-=SO32-+2CO2↑+2H2O
B.控制pH为9~10,用NaClO溶液将含NaCN的废水中的CN-氧化为两种无污染的气体:
2CN-+5ClO-+2H+=N2↑+2CO2↑+5Cl-+H2O
C.已知硫酸铅难溶于水,也难溶于硝酸,却可溶于醋酸铵溶液中,形成无色溶液。
当Pb(CH3COO)2溶液中通入H2S气体时有黑 色沉淀生成:Pb2++H2S=PbS↓+2H+
色沉淀生成:Pb2++H2S=PbS↓+2H+
D.CuSO4溶液与过量浓氨水反应:Cu2++4NH3·H2O=[Cu(NH3)4]2++4H2O
科目:高中化学 来源:2017届山东省泰安市高三上学期期中化学试卷(解析版) 题型:选择题
CuSO4、Fe2(SO4)3、H2SO4的混合溶液100 mL,已知溶液中阳离子的浓度相同(不考虑水解),且SO42-的物质的量浓度为6 mol·L-1,则此溶液最多溶解铁粉的质量为
A.5.6g B.11.2g C.22.4g D.33.6g
查看答案和解析>>
科目:高中化学 来源:2017届辽宁省高三第三次月考化学试卷(解析版) 题型:选择题
下图是实验室制取气体的装置,其中发生装置相同,干燥和集气装置有两套,分别用图1和图2表示。下列选项中正确的是( )

选项 | 发生装置中的药品 | 干燥和集气装置 |
A | 氧化钙和浓氨水 | 图1 |
B | 大理石和稀盐酸 | 图1 |
C | 铜和稀硝酸 | 图2 |
D | 电石和饱和食盐水 | 图2 |
查看答案和解析>>
科目:高中化学 来源:2017届江西省、兴国三中等四校高三上第一次联考化学卷(解析版) 题型:实验题
为了在实验室利用工业原料制备少量氨气,有人设计了如下装置(图中夹持装置均已略去)。
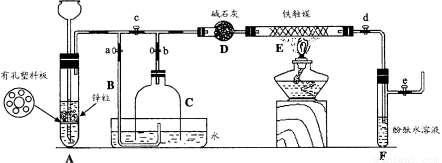
[实验操作]
① 检查实验装置的气密性后,关闭弹簧夹a、b、c、d、e。在A中加入锌粒,向长颈漏斗注入一定量稀硫酸。打开弹簧夹c、d、e,则A中有氢气发生。在F出口处收集氢气并检验其纯度。
② 关闭弹簧夹c,取下截去底部的细口瓶C,打开弹簧夹a,将氢气经导管B验纯后点燃,然后立即罩上无底细口瓶C,塞紧瓶塞,如图所示。氢气继续在瓶内燃烧,几分钟后火焰熄灭。
③ 用酒精灯加热反应管E,继续通氢气, 待无底细口瓶C内水位下降到液面保持不
待无底细口瓶C内水位下降到液面保持不 变时,打开弹簧夹b,无底细口瓶C内气体经D进入反应管E,片刻后F中的溶液变红。
变时,打开弹簧夹b,无底细口瓶C内气体经D进入反应管E,片刻后F中的溶液变红。
回答下列问题:
(1)检验氢气纯度的目的是 。
(2)C瓶内水位下降到液面保持不变时,A装置内发生的现象是 ,防止了实验装置中压强过大。此时再打开弹簧夹b的原因是 ,C瓶内气体的成份是 。
(3)在步骤③中,先加热铁触媒的原因是 。反应管E中发生反应的化学方程式是 。
查看答案和解析>>
科目:高中化学 来源:2017届江西省、兴国三中等四校高三上第一次联考化学卷(解析版) 题型:选择题
某研究性学习小组在整理实验室化学试剂时,发现一瓶盛有无色溶液的试剂,标签破损,如图.某同学根据中学化学知识,对该溶液中的溶质成分进行如下预测和验证,其中错误的是(包括预测物质的化学式、检验需要的试剂、操作、现象及结论)( )

选项 | 预测物质的化学式 | 检验需要的试剂 | 操作、现象及结论 |
A | Na2SO4 | 稀盐酸、氯化钡溶液 | 取少量该溶液于试管中,滴入稀盐酸,若无明显现象,再滴入氯化钡溶液,如果产生白色沉淀,则原溶液是Na2SO4溶液 |
B | Na2CO3 | 稀盐酸、澄清的石灰水 | 取少量该溶液于试管中,滴入足量稀盐酸,如果产生的无色气体能使澄清的石灰水变浑浊,则原溶液一定是Na2CO3溶液 |
C | Na2SO3 | 稀盐酸、澄清的石灰水、品红溶液 | 取少量该溶液于试管中,滴入足量稀盐酸,如果产生的无色气体既能使澄清的石灰水变浑浊,还能使品红溶液褪色,则原溶液是Na2SO3溶液 |
D | Na2SiO3 | 过量稀盐酸 | 取少量该溶液于试管中,滴入稀盐酸,产生白色胶状沉淀,盐酸过量时沉淀不溶解,则原溶液是Na2SiO3溶液 |
查看答案和解析>>
科目:高中化学 来源:2017届福建省高三上期中化学试卷(解析版) 题型:填空题
钠、钾的碘化物在生产和科学实验中有十分重要的应用。工业利用碘、NaOH和铁屑为原料可生产碘化钠,其生产流程如图所示:
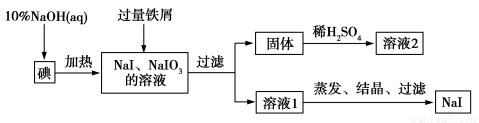
(1)NaOH溶液和碘反应时需要严格控制温度,如果温度过低,会生成碘的低价副产品NaIO。若NaOH溶液和碘反应时所得溶液中IO 与IO-的物质的量之比为1∶1,则该反应的离子方程式为 。
与IO-的物质的量之比为1∶1,则该反应的离子方程式为 。
(2)生产流程中加入过量铁屑的目的是__________________,过滤所得固体中除剩余铁屑外,还有红褐色固体,则加入铁屑时发生反应的化学方程式是__________________。
(3)溶液2中除含有H+外,一定含有的阳离子是_______________;试设计实验证实该金属阳离子的存在:___________________。
(4)溶液2经一系列转化可以得到草酸亚铁晶体(FeC2O4·2H2O),称取3.60 g草酸亚铁晶体(相对分子质量是180)用热重法 对其进行热分解,得到剩余固体的质量随温度变化的曲线如图所示:
对其进行热分解,得到剩余固体的质量随温度变化的曲线如图所示:

①分析图中数据,根据信息写出过程I发生的化学方程式:____________ ______。
②300℃时剩余固体只有一种且是铁的氧化物,试通过计算确定该氧化物的化学式:______________。
查看答案和解析>>
科目:高中化学 来源:2017届福建省高三上期中化学试卷(解析版) 题型:选择题
将由NaOH、BaCl2、Al2(SO4)3三种固体组成的混合物溶于足量的水中,充分溶解,向混合溶液中滴加1mol·L﹣1的稀硫酸,加入稀硫酸的体积与生成沉淀的质量关系如图所示.下列有关判断不正确的是( )
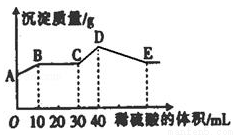
A.AB段发生反应的离子方程式为:Ba2++SO42—═BaSO4↓
B.E点对应横坐标稀硫酸的体积为70 mL
C.D点表示的沉淀的化学式为Al(OH)3、BaSO4
D.E点沉淀比A点沉淀质量大2.33g
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省等三校高二上期中化学卷(解析版) 题型:实验题
某化学学习小组在实验室模拟工业法制取Br2,装置如图所示。
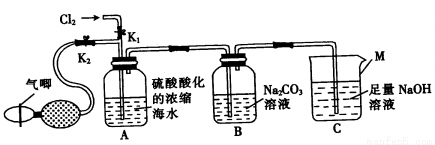
(1)仪器M的名称是________。
(2)实验室制取Cl2在通入装置A之前_______(填“需要”或“不需要”)除杂。
(3)实验前检査装置气密性的方法是_______________。
(4)反应过程中Br2在装置B中与Na2CO3反应生成NaBr和NaBrO3。为使装置A中产生的Br2尽可能被吸收,可采取的合理措施是_____________。
(5)反应结束后,取下装置B,向装置B中加入稀H2SO4会生成Br2,该反应的离子方程式为______________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年青海师大附中高一上期中化学试卷(解析版) 题型:选择题
下列离子方程式正确的是
A.CH3COOH溶液与NaOH溶液反应:H++OH-═H2O
B.碳酸氢钠溶液中加盐酸 CO32-+2H+=CO2+H2O
C.氢氧化钠溶液中加硫酸镁 2OH- 十Mg2+ =Mg(OH)2
D.氢氧化钡溶液中加硫酸 OH-+H+ =H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com