
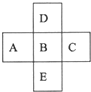
分析 A元素能与氧元素形成化合物AO2,AO2中氧的质量分数为50%,则A元素的相对分子质量为32,且A原子中质子数等于中子数,则其质子数为16,故A为S元素,结合元素在周期表中的位置可推知B为Cl、C为Ar、D为F、E为Br,以此来解答.
解答 解:A元素能与氧元素形成化合物AO2,AO2中氧的质量分数为50%,则A元素的相对分子质量为32,且A原子中质子数等于中子数,则其质子数为16,故A为S元素,可推知B为Cl、C为Ar、D为F、E为Br,则A为S元素,其原子序数为16,其氧化物除了SO2外还有SO3;B元素为Cl元素,E的单质为Br2,与C(Ar)原子具有相同核外电子排布的微粒为Cl-(Cl-离子结构示意图为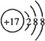 ),还有S2-、K+、Ca2+等,具有相同电子排布时核外电子数均为18,
),还有S2-、K+、Ca2+等,具有相同电子排布时核外电子数均为18,
故答案为:16;SO3;Cl;Br2;Cl-、S2-.
点评 本题考查位置、结构与性质的应用,为高频考点,把握元素的位置、原子结构推断元素为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大.


 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案科目:高中化学 来源: 题型:选择题
| A. | 金属性逐渐增强 | |
| B. | 化合价逐渐升高 | |
| C. | 失电子能力逐渐减弱 | |
| D. | 最高价氧化物对应的水化物碱性逐渐减弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 组别 | 10%硫酸体积/mL | 温度/℃ | 其他物质 |
| Ⅰ | 2mL | 20 | / |
| Ⅱ | 2mL | 30 | / |
| Ⅲ | 1mL | 20 | 1mL蒸馏水 |
| Ⅳ | A | 20 | B |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
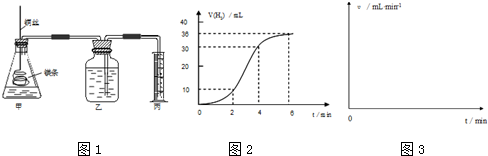
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 少量二氧化碳通入“水玻璃”中:C02+SiO32-+H20═C032-+H2SiO3↓ | |
| B. | 氨水滴入 AlCl3 溶液中:Al3++30H-═Al(0H)3↓ | |
| C. | 铝溶解在NaOH溶液中:2Al+2OH-+6H2O═2[Al(OH)4]-+3H2↑ | |
| D. | Al2O3溶于 NaOH 溶液中:Al2O3+2OH-+3H2O=2[Al(0H)4]- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若HnXOm为强酸,则X的氢化物溶于水一定显酸性 | |
| B. | 若X(OH)n为强碱,则Y(OH)n也一定为强碱 | |
| C. | 若X元素形成的单质是X2,则Y元素形成的单质也一定是Y2 | |
| D. | 若Y的最高正化合价为+m,则X的最高正化合价一定为+m |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com