
下列实验中能证明某气体为SO2的是 ( )
①使澄清石灰水变浑浊 ②使湿润的蓝色石蕊试纸变红 ③使品红溶液褪色 ④通入足量NaOH溶液中,再滴加BaCl2溶液,有白色沉淀生成,该沉淀溶于稀盐酸 ⑤通入溴水中,能使溴水褪色,再滴加Ba(NO3)2溶液有白色沉淀产生
A.都能证明 B.都不能证明
C.③④⑤均能证明 D.只有⑤能证明
科目:高中化学 来源: 题型:
对于:2C4H10(g) + 13O2(g) = 8CO2(g) + 10H2O(l) △H=-5800kJ/mol 叙述错误的是( )
A.该反应的反应热为△H= -5800kJ/mol,是放热反应。
B.该反应的△H与各物质的状态有关,与化学计量数也有关。
C.该式的含义为:25℃、101kPa,2mol C4H10气体完全燃烧生成CO2和液态水时放出热量5800kJ。
D.由该反应的热化学方程式可知丁烷的燃烧热为5800kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度、一定体积下,下列叙述不能作为可逆反应A(g)+3B(g)  2C(g)达到平衡状态标志的是( )
2C(g)达到平衡状态标志的是( )
①C的生成速率与C的消耗速率相等 ②单位时间内生成a mol A,同时生成3a mol B
③A、B、C的浓度不再变化 ④C的物质的量不再变化
⑤混合气体的总压强不再变化 ⑥混合气体的总物质的量不再变化
⑦单位时间消耗a mol A,同时生成3a mol B ⑧A、B、C的分子数之比为1∶3∶2
A.②⑧ B.④⑦ C.①③ D.⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学小组在实验室模拟用软锰矿(主要成分MnO2,杂质为铁及铜的化合物等)制备高纯碳酸锰,过程如下(部分操作和条件略):
① 缓慢向烧瓶中通入过量混合气进行“浸锰”操作,主要反应原理为:
SO2+ H2O = H2SO3 ; MnO2+ H2SO3 = MnSO4+ H2O
(铁浸出后,过量的SO2 会将Fe3+还原为Fe2+)
② 向“浸锰”结束后的烧瓶中加入一定量纯MnO2粉末。
③ 再用Na2CO3溶液调节pH为3.5左右,过滤。
④ 调节滤液pH为6.5~7.2 ,加入NH4HCO3 ,有浅红色的沉淀生成,过滤、洗涤、干燥,得到高纯碳酸锰。回答下例问题:
(1)步骤②中加入一定量纯MnO2粉末的主要作用是将Fe2+氧化为Fe3+ ,将过量的SO2氧化除去,相应反应的离子方程式为 。
(2)查阅表1,步骤③中调pH为3.5时沉淀的主要成分是 。
表1:生成相应氢氧化物的pH
| 物质 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Cu(OH)2 |
| 开始沉淀pH | 2.7 | 7.6 | 8.3 | 4.7 |
| 完全沉淀pH | 3.7 | 9.6 | 9.8 | 6.7 |
(3)步骤③中所得的滤液中含有Cu2+,可添加过量的难溶电解质MnS除去Cu2+,经过滤,得到纯净的MnSO4。用平衡移动原理解释加入MnS的作用_________________。
(4)④中加入NH4HCO3 后发生反应的离子方程式是____________________。
(5)检验④中沉淀是否洗涤干净的方法是 。
(6)现有常温下的四种溶液:
①0.1mol·L-1 NH4Cl溶液
②0.1mol·L-1 NH4Cl和0.1mol·L-1 NH3·H2O的混合溶液(显碱性)
③0.1mol·L-1 NH3·H2O
④0.1mol·L-1 NH4Cl和0.1mol·L-1 HCl
下例说法正确的有 (填字母序号)
A. NH4+离子浓度从大到小的顺序为②>④>①>③
B.溶液的pH从大到小的顺序为③>①>②>④
C.溶液中的离子总浓度从大到小的顺序为④>①>②>③
查看答案和解析>>
科目:高中化学 来源: 题型:
将SO2分别通入下表所列的溶液中,填写有关问题。
| 反应物 | 溴水 | 酸性 KMnO4 溶液 | 氢硫酸 (H2S溶液) | 滴有酚酞的 NaOH溶液 | 石蕊试液 | 品红 溶液 |
| 反应现象 | 褪色 | 褪色 | 有淡黄色 沉淀生成 | 褪色 | 变红 | 褪色 |
| SO2的性质 | 还原性 | 还原性 | 氧化性 |
| 酸性 | 漂白性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
某兴趣小组在实验室用铜和硫酸为原料,采用多种方法制取硫酸铜,制备方法如下:
方法一
(1)浓硫酸试剂瓶上适合贴上的标签是________(填序号)。
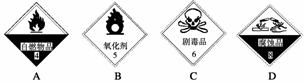
(2)甲同学取6.4 g铜片和10 mL 18 mol·L-1浓硫酸,放在试管中共热时发现,铜与热的浓硫酸反应后并没有得到预期的蓝色溶液,而是在试管底部看到灰白色沉淀。甲同学为了验证其中灰白色沉淀的主要成分,设计下列实验:
实验步骤:倾倒掉上层液体后,向所得灰白色的固体中加入适量蒸馏水,边加边搅拌。
实验现象:_____________________________________________________________。
实验结论:所得灰白色固体的化学式为__________。
(3)乙还观察到加热过程中,试管内壁上部析出少量淡黄色固体物质,持续加热,淡黄色固体物质又慢慢地溶于浓硫酸而消失。淡黄色固体消失的原因是(用化学方程式回答)________________________________________________________________________。
直到最后反应完毕,发现试管中还有铜片剩余,乙根据自己所学的化学知识,认为试管中还有硫酸剩余。他这样认为的理由是______________________________________。
方法二
(4)丙同学认为甲设计的实验方案不好,他自己设计的思路是2Cu+O2 2CuO,CuO+H2SO4===CuSO4+H2O。
2CuO,CuO+H2SO4===CuSO4+H2O。
对比甲的方案,你认为丙同学的优点是①_____________________________________;
②________________________________________________________________________。
方法三
(5)丁同学取一铜片和稀硫酸放在试管中,再向其中滴入双氧水发现溶液逐渐呈蓝色,写出反应的化学方程式_______________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列措施或叙述不合理的是 ( )
A.用SO2漂白纸浆和草帽辫 (2013·广东理综,11A)
B.用硫酸清洗锅炉中的水垢 (2013·广东理综,11B)
C.将浓硫酸滴到蔗糖表面,固体变黑膨胀,说明浓硫酸有脱水性和强氧化性
(2013·广东理综,23A)
D.Na2SO3与H2O2的反应为氧化还原反应 (2013·天津理综,1B)
查看答案和解析>>
科目:高中化学 来源: 题型:
烟气脱硫是控制二氧化硫污染的主要技术手段。
(1)利用海水脱硫是一种有效的方法,其工艺 流程如图所示:
流程如图所示:
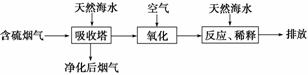
某研究小组为探究提高含硫烟气中SO2的吸收效率的措施,进行了天然海水吸收含硫烟气的模拟实验,实验结果如图所示:
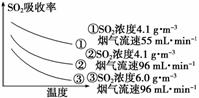
①根据图示实验结果,为了提高一定浓度含硫烟气中SO2的吸收效率,下列措施正确的是________(填序号)。
A.降低通入含硫烟气的温度
B.减小通入含硫烟气的流速
C.减少天然海水的进入量
D.在天然海水中加入生石灰
②天然海水吸收了含硫烟气后会溶有H2SO3,使用空气中的氧气将其氧化,写出该反应的离子方程式:__________________________________________________________
________________________________________________________________________。
③该小组采用如图装置在实验室测定烟气中SO2的体积分数(假设实验在标准状况下进行)。

上述装置连接的顺序是原料气→________(填a、b、c、d、e)。下列试剂中(浓度、体积一定),可以用来代替试管中的碘淀粉溶液的是________(填编号)。
A.酸性KMnO4溶液 B.NaOH溶液
C.溴水 D.氨水
(2)石灰石石膏湿法烟气脱硫工艺技术的工作原理是烟气中的二氧化硫与浆液中的碳酸钙及鼓入的空气反应生成石膏(CaSO4·2H2O)。写出该反应的化学方程式:________________________________________________________________________
___________________________________________________ _____________________。
_____________________。
某电厂用煤300 t(煤中含硫质量分数为2.5%),若燃烧时煤中的硫全部转化成二氧化硫,用该方法脱硫时有96%的硫转化为石膏,则可生产石膏________ t。
答案 (1)①ABD ②2H2SO3+O2===4H++2SO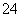
③c→d→b→a→e AC
(2)2CaCO3+2SO2+O2+4H2O===2(CaSO4·2H2O)+2CO2 38.7
查看答案和解析>>
科目:高中化学 来源: 题型:
关于下列物质的说法,正确的是( )

A.三者含有的官能团的种类相同 B.乙和丙中的-OH性质相同
C.甲和乙互为同分异构体 D.甲和丙互为同分异构体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com