
 以下为苯的取代反应的探究实验.
以下为苯的取代反应的探究实验.| 试剂 |
| 操作 |
 ;吸收溴和苯的蒸气.
;吸收溴和苯的蒸气.

 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案科目:高中化学 来源: 题型:

A、a点对应的溶液中:NH
| ||||||
B、b点对应的溶液中:Na+、S2-、SO
| ||||||
C、c点对应的溶液中:Ag+、Ba2+、K+、NO
| ||||||
D、d点对应的溶液中:K+、S2-、I-、CO
|
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
A、食盐中阴离子的结构示意图为: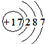 |
| B、蔗糖和醋酸都是弱电解质 |
C、“84消毒液”中有效成分NaClO的电子式为: |
| D、明矾溶液水解可制得Al(OH)3胶体,用于杀菌消毒 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 结晶 |
| 精制 |
| 电解 |

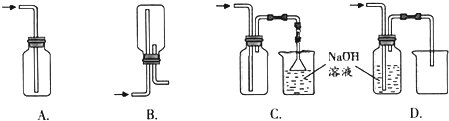
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com