
NH3极易溶于水,与此性质无关的是
A.NH3与水形成分子间氢键 B.NH3是极性分子
C.NH3相对分子质量小,范德华力小 D.NH3会与水发生反应
科目:高中化学 来源:2014-2015学年福建省漳州市高三3月质量检查化学试卷(解析版) 题型:填空题
(14分)目前机动车使用的电池品种不少,其中铅蓄电池的使用量最大。
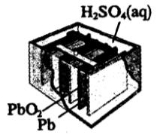
I.铅蓄电池的电极材料分别是Pb和PbO2,电解质溶液为稀硫酸。铅蓄电池充放电的总反应方程式为:
PbO2+Pb+2H2SO4  2PbSO4+2H2O,
2PbSO4+2H2O,
请根据上述情况判断:
(1)电池的负极材料是 。
(2)充电时,铅蓄电池阳极的电极反应式为 。
Ⅱ.铅蓄电池使用量的急速增加引起铅污染日益严重,工业上从废铅蓄电池的铅膏回收铅的一种工艺流程如下:
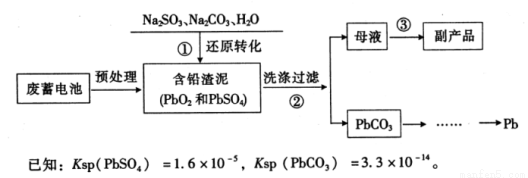
请回答下列问题:
(3)为提高步骤①的化学反应速率,你认为可采取的措施是 (写一条即可)。
(4)写出步骤①中PbSO4转化为PbCO3反应的平衡常数表达式:K = 。
(5)步骤①中发生氧化还原反应的化学方程式为 。
(6)步骤③从母液可获得的副产品为 (写化学式)。
(7)已知:PbCO3在一定条件下可制得PbO,PbO通过进一步反应可制得Pb,写出一个由PbO生成Pb的化学方程式: 。
查看答案和解析>>
科目:高中化学 来源:2014-2015四川省资阳市高一上学期学期期末化学试卷(解析版) 题型:选择题
下列物质转化关系中,需要加入氧化剂才能实现的是
A.Na2O2 →O2 B.MnO4-→Mn2+ C.Fe2+→Fe3+ D.CO2→HCO3-
查看答案和解析>>
科目:高中化学 来源:2014-2015四川省资阳市高二上学期学期期末化学试卷(解析版) 题型:选择题
现有三种元素的基态原子的电子排布式如下:① [Ne]3s23p4;② 1s22s22p63s23p3;③1s22s22p5。则上述三种原子的第一电离能大小关系正确的是
A.②>①>③
B.③>①>②
C.③>②>①
D.①>②>③
查看答案和解析>>
科目:高中化学 来源:2014-2015四川省资阳市高二上学期学期期末化学试卷(解析版) 题型:选择题
下列措施肯定能使化学反应速率增大的是
①增大反应物的量 ②增大压强 ③升高温度 ④使用正催化剂
A.①②③ B.③④ C.②③④ D.①②③④
查看答案和解析>>
科目:高中化学 来源:2014-2015上海市高一上学期期末考试化学试卷(解析版) 题型:实验题
为了探究Cl2、SO2同时通入H2O中发生的反应,某校化学兴趣小组同学设计了如下图所示的实验装置。
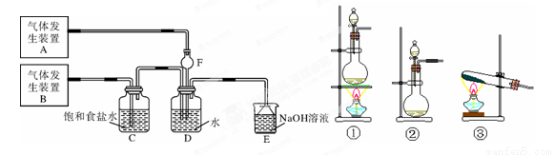
(1)该组同学为了制取Cl2,SO2气体,现采用Na2SO3与70%的浓硫酸为原料制取SO2,采用MnO2和浓盐酸(12mol/L)为原料制取Cl2。在此实验中,发生装置B应选择三种装置中的___________(选填序号),F的作用是_____________。
(2)D装置中主要反应的离子方程式为__________________________。
(3)为检验通入D装置中的Cl2是否过量,该组同学取适量D溶液滴加至盛有少量紫色石蕊的试管中,若出现___________现象,则Cl2过量,此时E中发生的离子反应方程式为______________________,若D中出现__________________实验现象,则氯气不过量。
查看答案和解析>>
科目:高中化学 来源:2014-2015上海市高一上学期期末考试化学试卷(解析版) 题型:选择题
碳酸铜和碱式碳酸铜[Cu2(OH)2CO3]均可溶于HCl,转化为氯化铜。在高温下这两种化合物均能分解生成氧化铜。溶解28.4g的上述混合物,消耗1.0 mol/L盐酸500mL。灼烧等量的上述混合物,得到氧化铜的质量为
A.35g B.30g C.20g D.15g
查看答案和解析>>
科目:高中化学 来源:2014-2015上海市高一上学期期末考试化学试卷(解析版) 题型:选择题
可以证明某化合物一定含有离子键的性质是
A.熔融状态能导电 B.具有较高的熔点
C.可溶于水 D.溶于水能导电
查看答案和解析>>
科目:高中化学 来源:2014-2015学年陕西省西安市高三下学期第一次月考理综化学试卷(解析版) 题型:选择题
下列液体均处于25°C,有关叙述正确的是
A.AgCl在同浓度的CaCl2和NaCl溶液中的溶解度相同
B.某物质的溶液pH<7,则该物质一定是酸或强酸弱碱盐
C.pH=4.5的番茄汁中c(H+)是pH=6.5的牛奶中pH=4.5的番茄汁中c(H+)是pH=6.5的牛奶中的100倍
D.pH=5.6的CH3COOH与CH3COONa混合溶液中,c(Na+)>c(CH3COO-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com