
| A、7 | B、8 | C、9 | D、10 |


科目:高中化学 来源: 题型:
| A、铝箔熔化,失去金属光泽 |
| B、铝在空气中能很快形成氧化膜 |
| C、氧化铝的熔点比铝高 |
| D、氧化铝与盐酸不反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、同浓度下列溶液中:①(NH4)2SO4 ②NH4HCO3 ③NH4Cl ④NH3?H2O,c(NH4+)由大到小的顺序是:①>③>②>④ |
| B、常温时,将等体积的盐酸和氨水混合后pH=7,则c(NH4+)>c(Cl-) |
| C、0.2mol?L-1Na2CO3溶液中:c(OH-)=c(HCO3-)+c(H+)+c(H2CO3) |
| D、0.01mol?L-1的NH4Cl溶液与0.05mol?L-1的NaOH溶液等体积混合:c(Cl-)>c(NH4+)>c(Na+)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Cu2S既是氧化产物,又是还原产物 |
| B、产物中的SO42-部分有一部分是氧化产物 |
| C、5mol FeS2发生反应时,有10mol电子转移 |
| D、FeS2只做还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、草酸氢钾溶液呈酸性,在0.1mol?L-1 KHC2O4溶液中:c(C2O42-)>c(H2C2O4) |
| B、在小苏打水溶液中:c(Na+)+c(H+)=c(HCO3-)+c(CO32-)+c(OH-) |
| C、相同温度下,1mol?L-1氨水溶液与0.5mol?L-1氨水溶液中,c(OH-)之比是2:1 |
| D、当氨水与盐酸恰好完全反应时,c(NH4+)>c(Cl-)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
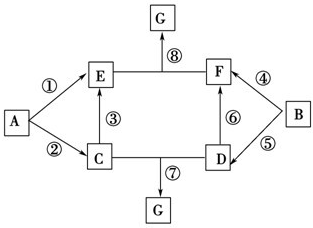 A~G的转化关系如图所示(部分反应物、产物和反应条件未标出).
A~G的转化关系如图所示(部分反应物、产物和反应条件未标出).查看答案和解析>>
科目:高中化学 来源: 题型:
| M | |
| T |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com